Respiratory Physiology
Prof. Zaid Al-Madfai
RESPIRATORY PHYSIOLOGY
The process of respiration is divided into four categories:
1- Pulmonary ventilation.
2- Diffusion of oxygen and CO
2
between alveoli and tissues.
3- Transport of oxygen and CO
2
in body fluids to and from cells.
4- Regulation of respiration
Pulmonary Ventilation
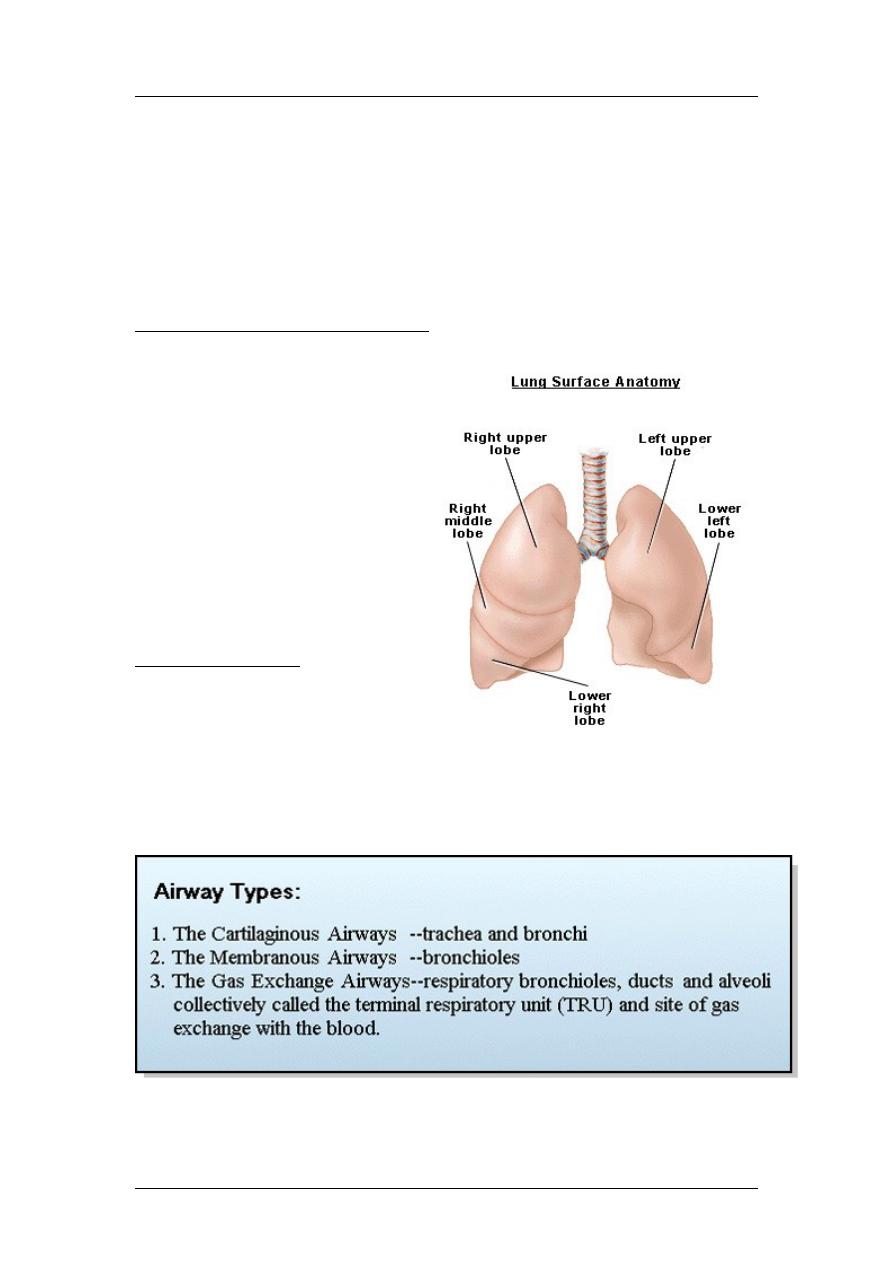
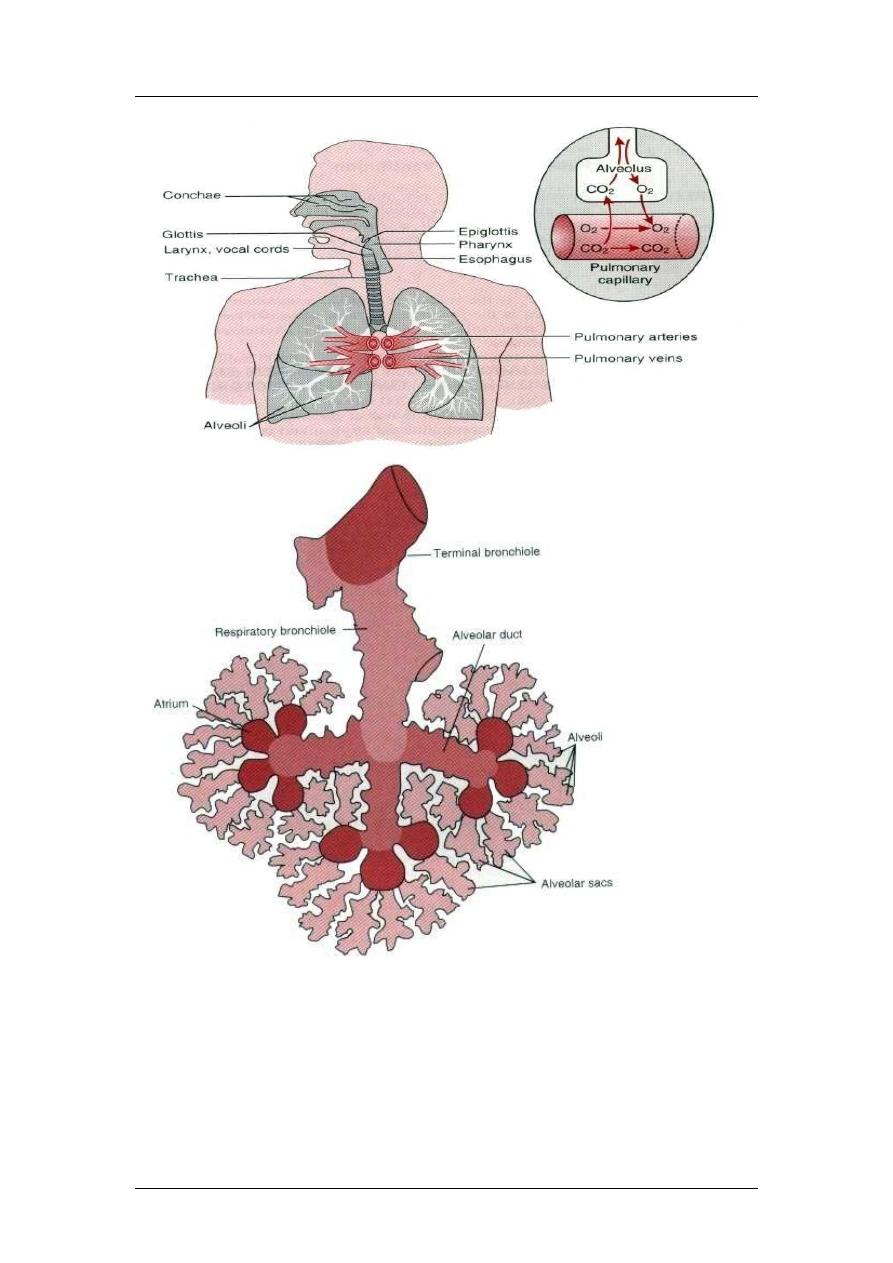
Anatomy of the Respiratory System
The respiratory system includes
the lungs, the conducting
airways that direct air to the gas
exchange sites (alveoli), certain
parts of the central nervous
system, and the muscles of the
chest wall and the diaphragm
that are responsible for inflation
and deflation of the lungs. The
lungs fill most of the thoracic
cavity except for the space
occupied by the heart and major
blood vessels.
Tissues of the Lung
The normal adult human lung
weighs about 1000g and
consists of about 50% blood
and 50% tissue by weight.
About 10% of the total lung volume is composed of various types of
conducting airways and some connective tissue. The remaining 90% is the
respiratory or gas exchange portion of the lung, composed of alveoli and
supporting capillaries.
1
Respiratory Physiology
Prof. Zaid Al-Madfai
Airway Anatomy
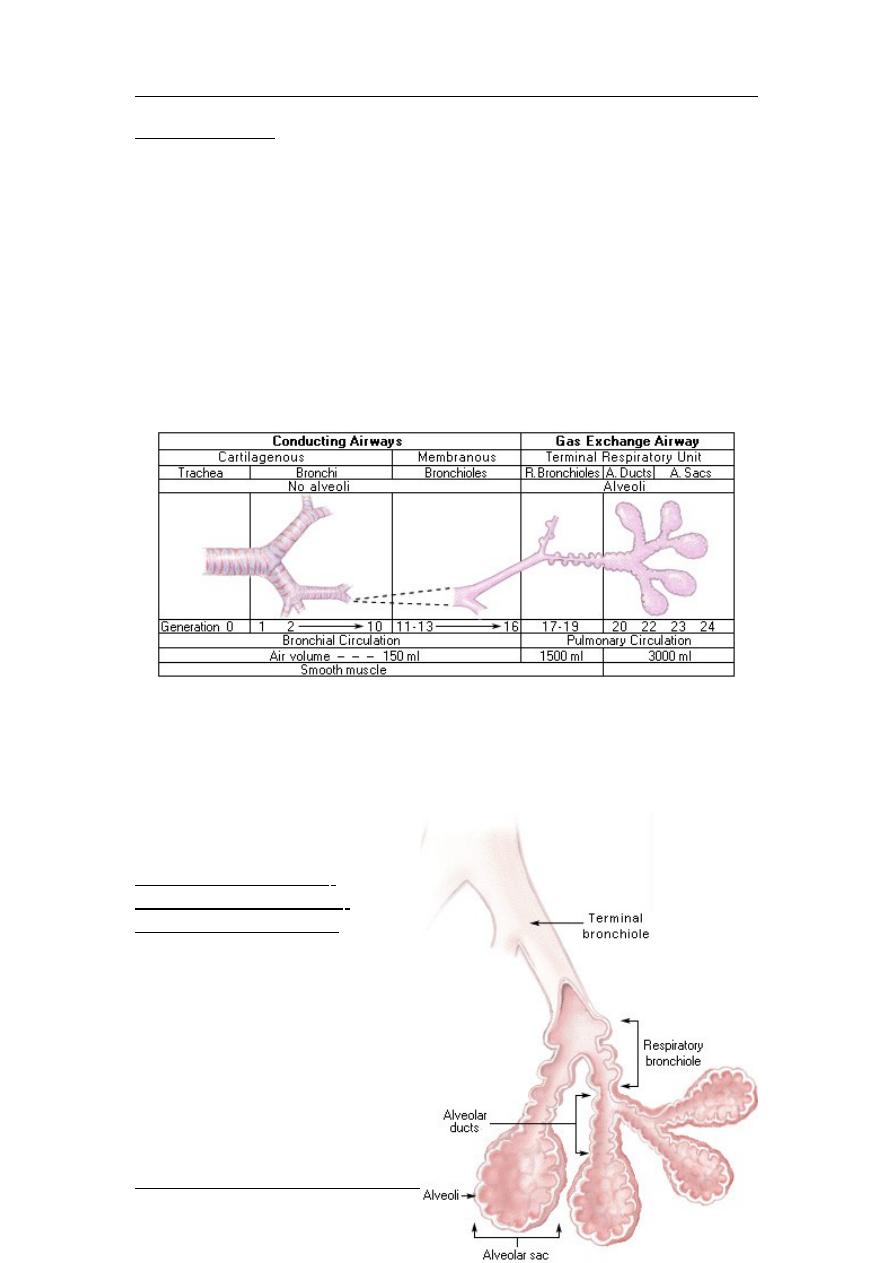
The conducting airways consist of a series of rapidly branching tubes
(conduits) that become narrower, shorter, and more numerous as they
penetrate deeper into the lung. After about 23 to 25 orders of branching, the
airways terminate in alveoli. The airway can be classified longitudinally or
sequentially and anatomically into three distinct types.
Starting at the trachea, the airways branch in a dichotomous fashion both
symmetrically and asymmetrically. The fibrous layer is encircled by smooth
muscle innervated by parasymphathetic nerves that cause contraction of the
airway smooth muscle. This is termed bronchoconstriction. The extent and
importance of sympathetic nervous system innervation in the initiation of
bronchial smooth muscle relaxation is unclear. Each generation of airway
branching is assigned a number, with the trachea assigned zero (0).
The gas exchange airway may be reached in as few as 10 levels of branching,
but around 16th level of branching is more typical. From the trachea, the
airway diameter decreases with each new generation of branching. However,
the total cross-sectional area increases with each level of branching. As a
result, the linear velocity of airflow decreases with each order of branching, an
important consideration in
determining the distribution
of airway resistance.
Gas Exchange Airway:
Respiratory Bronchioles,
Alveolar Ducts and Sacs
The gas exchange airway is
the functional unit of the lung.
It consists of the respiratory
bronchioles, alveolar ducts,
and alveolar sacs, which
collectively comprise the
terminal respiratory unit
(TRU). The TRU is distal to
and a direct continuation of
2
Respiratory Physiology
Prof. Zaid Al-Madfai
the terminal bronchioles. It is the site of gas exchange with the pulmonary
capillary blood. The gas exchange airway typically begins at about the 19th
order of branching with the appearance of the respiratory bronchioles. The
distinguishing feature of TRU is the presence of alveoli. The structural
support for the TRU arises from the connective tissue framework of the lung.
Alveoli line the walls of both the respiratory bronchioles and alveolar ducts,
both of which are perfused with pulmonary capillary blood. Some smooth
muscle also is present in respiratory bronchioles and alveolar ducts. This
muscle can be stimulated by vasoactive substances in the pulmonary blood.
There are usually 2 to 5 orders of branching of both respiratory bronchioles
and alveolar ducts before the latter empty into an atrium consisting of one to
three dome-shaped alveolar sacs.
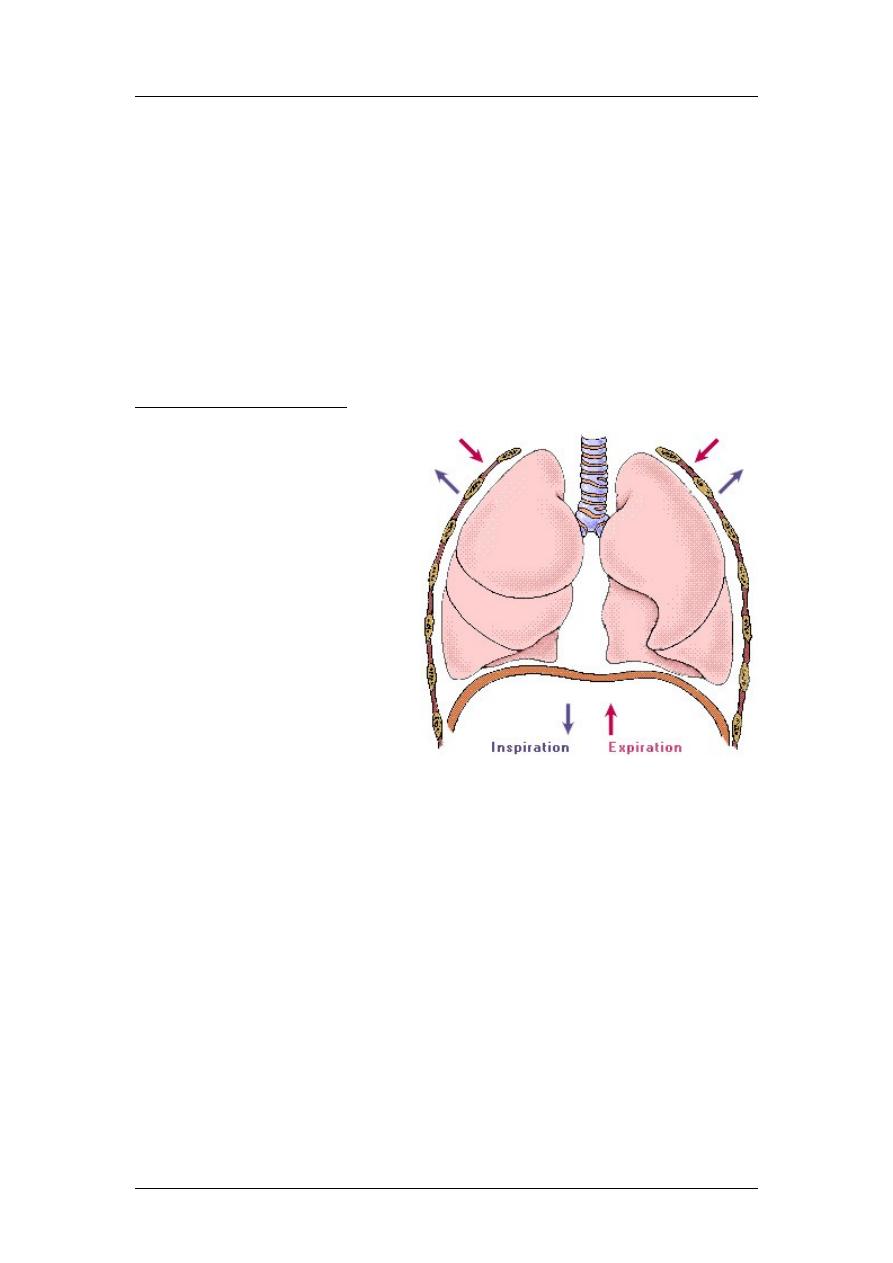
Mechanics of Ventilation
Air is delivered to alveoli as a
consequence of respiratory
muscle contraction. These
muscles include the
diaphragm and the external
intercostal muscles of the rib
cage and accessory
inspiratory muscles (scalenes
and sternocleidomastoids
which are not active in
eupnea). Contraction of these
muscles enlarges the thoracic
cavity, creating a
subatmospheric pressure in
the alveoli. Contraction of the
diaphragm leads to
downwards displacement of
the thoracic cavity and contraction of external intercostals muscles leads to
lifting of the thoracic cage leading to increase in the antero-posterior diameter.
As alveolar pressure declines, atmospheric air moves into the alveoli by bulk
flow until the pressure is equalized. The process of inflating the lung is called
inspiration. Expiration is usually passive, resulting from relaxation of the
inspiratory muscles and powered by elastic recoil of lung tissue that is
stretched during inspiration. With relaxation of the inspiratory muscles and
lung deflation, alveolar pressure exceeds atmospheric pressure, so gases flow
from the alveoli to the atmosphere by bulk flow. Active expiration is due to
internal intercostals muscles and the abdominal recti muscles.
3
Respiratory Physiology
Prof. Zaid Al-Madfai
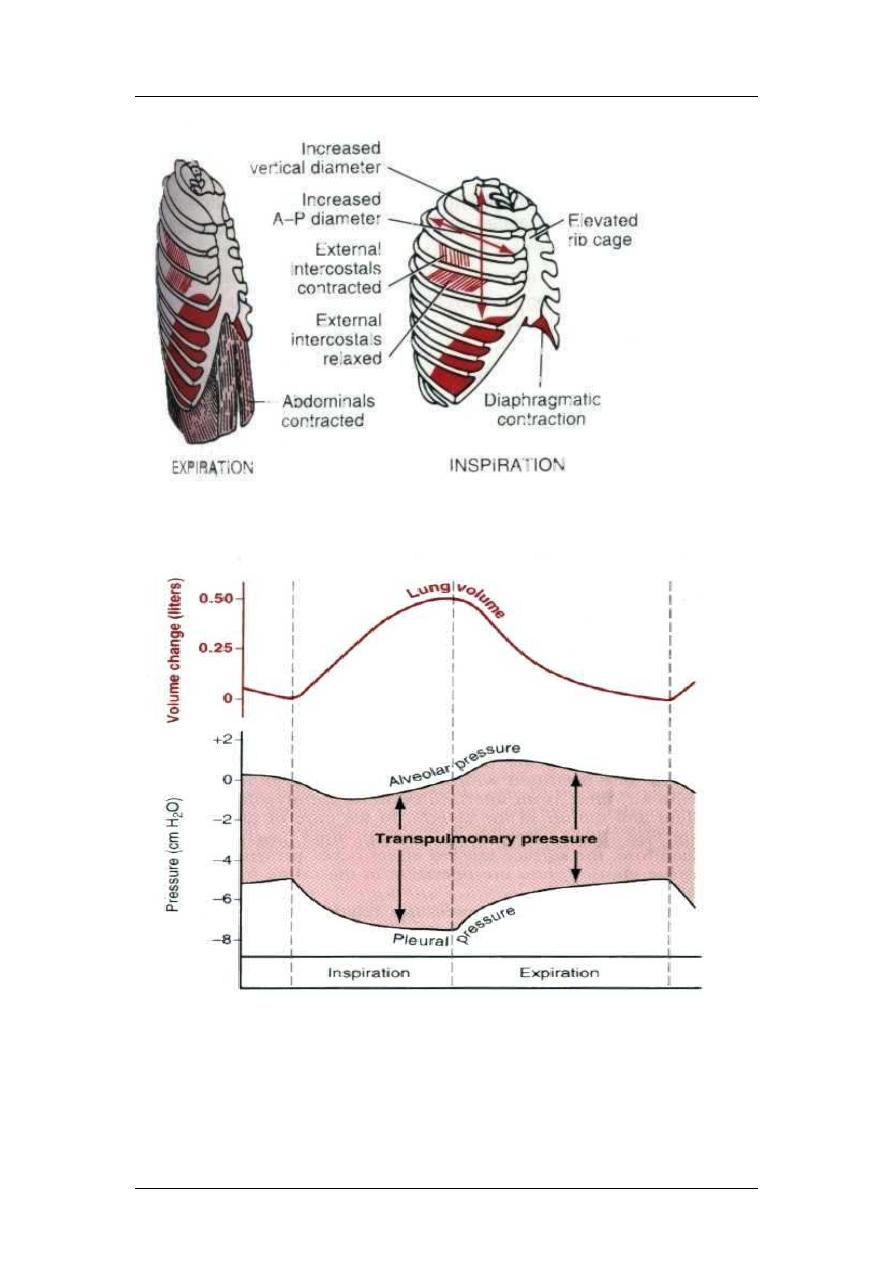
Pleural pressure is the pressure of the fluid in the thin space between the lung pleura
and the chest wall pleura. Pleural pressure [-5cmH2O to -7cmH2O]
Alveolar pressure is the pressure of the air inside the lung alveoli. The alveolar
Pressure [0 to -1 to 0, then 0 to +1 to 0]
Transpulmonary pressure [pressure difference between the alveolar pressure and the
pleural pressure]. It is the measure of the elastic forces that leads to collapse of the
lung and it is called the recoil pressure.
4

Respiratory Physiology
Prof. Zaid Al-Madfai
The Opposing Force of Pulmonary Elastance or Compliance
The lung is an elastic structure with an anatomical organization that promotes
its collapse to essentially zero volume, much like an inflated balloon. The term
elastic means a material deformed by a force tends to return to its initial shape
or configuration when the force is removed. While the elastic properties of the
lung are important to bring about expiration, they also oppose lung inflation.
As a result, lung inflation depends upon contraction of the inspiratory muscles.
The resistance to deformation (inflation) is termed elastance. However,
compliance is the preferred term to describe the elastic properties of the lung.
Compliance, as the recripocal of elastance, is a measure of the ease of
deformation (inflation).
Relationship of Elastance to Compliance
Compliance is measured as the
change in volume for a given
change in pressure. Thus, a
structure with high elastance
(very stiff) has a low
compliance. A term used as a
synonym for compliance is
distensibility. Accordingly, an
object with a high elastance
would exhibit a high resistance
to deformation and have a low
compliance or low
distensibility. On the other hand, an object with a high compliance distends
readily with little pressure. Thus, in a lung with a high compliance, a small
pressure change would result in a large volume change and the work
performed by the respiratory muscles to inflate the lung would be less than
normal. However, the expiratory force would also be less than normal in a
lung with high compliance.
Lung compliance
: Which equals to change in volume divided by change in
pressure (1 cm = 200 ml). That is, every time the transpulmonary pressure increases 1
centimeter of water, the lung volume, after 10 to 20 seconds, will expand 200
milliliters.
-
1/3 to overcome pleural pressure
-
2/3 to overcome surface tension
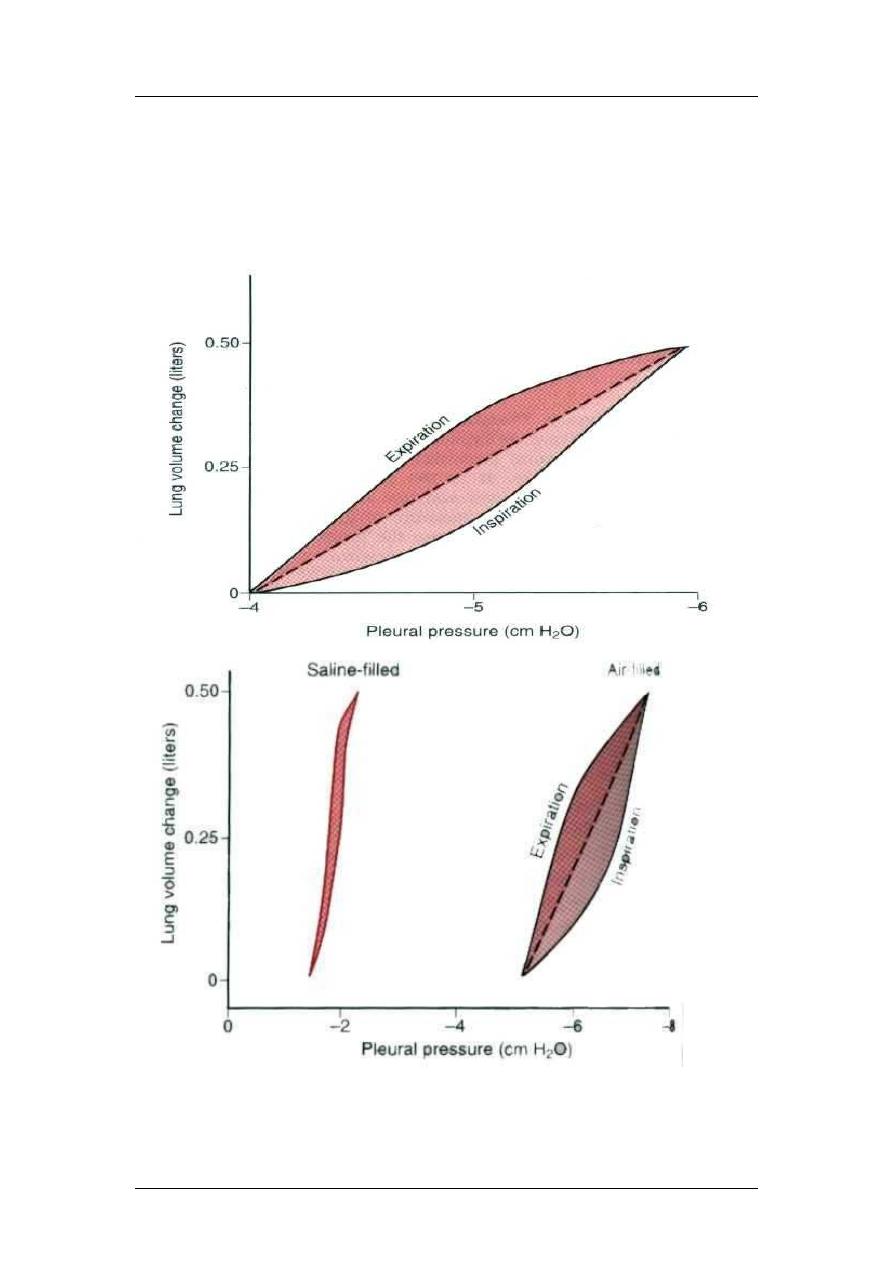
If the lung is removed from the thoracic cage, it closely resembles a collapsed
balloon. When pressure inside the lung equals outside pressure, or transmural pressure
is 0, lung volume is close to zero. Compliance of the lung can be obtained by plotting
lung relaxation or recoil pressure (x axis) as a function of lung volume (y axis).
Starting from essentially zero lung volume, a measured volume of air is put into the
lung and the recoil or relaxation pressure associated with the addition of that air
volume is recorded. When repeated in several steps by the sequential addition of
measured air volumes and recording of the corresponding recoil or relaxation
5
Respiratory Physiology
Prof. Zaid Al-Madfai
pressures, a compliance curve for the lung can be constructed. The slope of this plot is
lung compliance. Normally, lung compliance is measured under static conditions,
meaning no airflow is present at the time the relaxation (recoil) pressure is measured.
Effect of thoracic cage
Compliance of both lung + cage = 110 ml (instead of 200ml/cm)
Surface tension means the pulling force of fluid (as in rain drops). Surface tension is
defined as a manifestation of attracting forces between atoms or molecules.
6

Respiratory Physiology
Prof. Zaid Al-Madfai
Surfactant: The surface active agent in water and it consists of lipids, protein and ions.
Respiratory Distress Syndrome
Problems with high alveolar surface
tension are common in premature
infants. The fetal lung does not begin to
synthesize alveolar surfactant until about
the fourth month of gestation. Fetal lung
surfactant also is not fully functional
until about the seventh month of
gestation. Respiratory Distress
Syndrome (RDS) is related to non-
functional alveolar surfactant. RDS is
characterized by severe alveolar
instability, high alveolar surface tension, and high alveolar opening pressures.
The respiratory muscles of premature infants frequently cannot generate
sufficient pressures to open or inflate alveoli because of their high alveolar
surface tension. RDS in infants is manifested by a low lung compliance and
severe hypoxemia. Surfactant deficiency or inactivation can also occur in
adults who breathe 100% O
2
for prolonged periods, or who have prolonged
occlusion of the pulmonary artery, such as associated with heart-lung bypass
procedures. Constant-volume mechanical ventilation or prolonged hypoxia or
hypoxemia can also lead to surfactant inactivation.
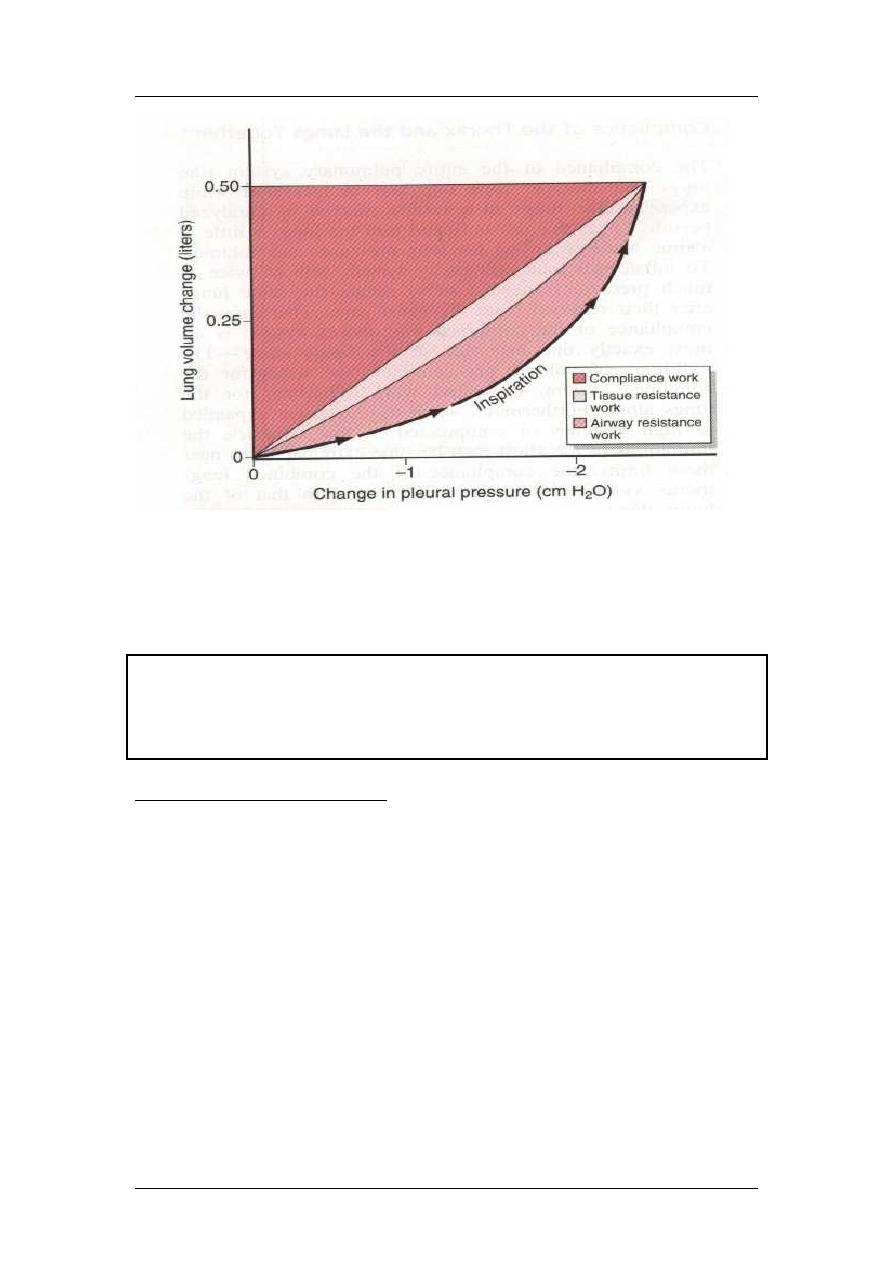
Work of breathing:
1- Compliance work: against elastic forces of lung + cage
2- Tissue resistance work: against viscosity of both lung and cage
3- Airway resistance work
7
Respiratory Physiology
Prof. Zaid Al-Madfai
During quite breathing, 3-5% of total energy of the body are spent for respiration,
while in heavy exercise, it increases up to 50 folds.
Lung volumes
Volumes
Capacities
1- Tidal vol. (500ml)
1- Inspiratory cap. (3500ml)
2- Inspiratory reserve vol. (3000ml)
2- Functional residual cap. (2300ml)
3- Expiratory reserve vol. (1100ml)
3- Vital cap. (4600ml)
4- Residual vol. (1200ml)
4- Total lung cap. (5800ml)
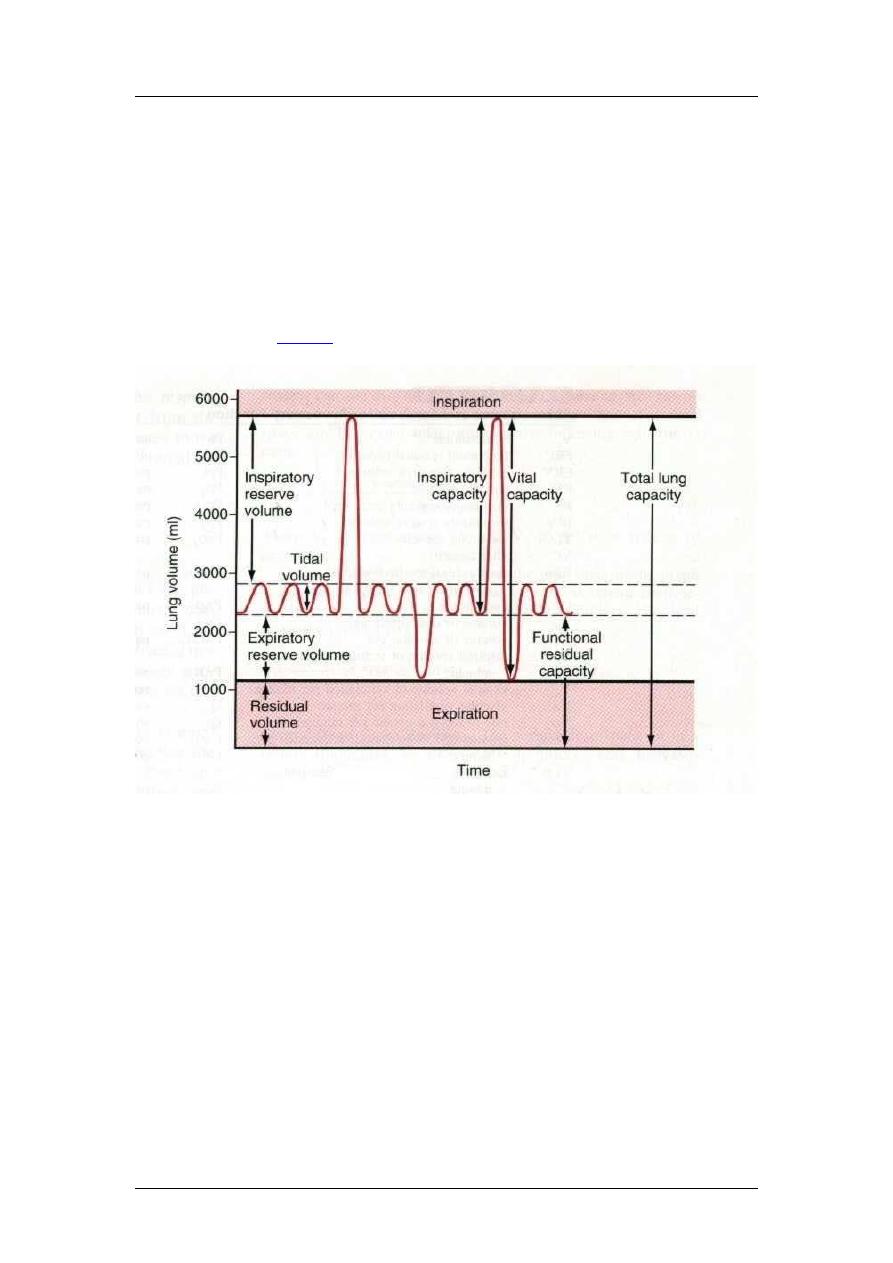
Lung Volumes and Capacities
Lung volumes measured by spirometry are basically anatomical measurements
of lung gas volumes. A lung volume refers to a basic volume of the lung,
whereas lung capacities, also a volume measurement, are the sum of two or
more basic lung volumes. The following lung volumes can be measured
directly or indirectly with a spirometer:
Tidal Volume (VT): volume of gas inspired or expired during a normal
spontaneous breath.
Inspiratory Reserve Volume (IRV): volume of gas that can be inspired at the
end of a spontaneous inspiration.
Expiratory Reserve Volume (ERV): volume of gas that can be expired at the
end of a spontaneous VT.
Residual Volume (RV): volume of air in lungs that cannot be forcefully
expired or the volume of air in lung at end of a vital capacity.
Vital Capacity (VC): maximum volume of gas that can be expired after a
maximal inspiration or IRV + VT + ERV.
8
Respiratory Physiology
Prof. Zaid Al-Madfai
Inspiratory Capacity (IC): the maximal volume of air that can be inspired
from normal end-expiration or VT + IRV
Functional Residual Capacity (FRC): total volume of air in the lung at end
of normal end-expiration or ERV + RV.
Total Lung Capacity (TLC): total volume of gas in lung at maximal end-
inspiration or VC + RV or IRV + VT + ERV + RV.
Note that RV cannot be measured directly with a spirometer because it is not
possible to expire this lung volume. Thus, any lung capacity that includes the
RV cannot be measured directly with a spirometer. To measure RV or FRC,
indirect gas
techniques or whole body plethysmography are used.
The minute respiratory volume: Total amount of new air moved into the respiratory
passages per minute and is equal to tidal volume (500 ml) multiplied by the
respiratory rate (12/min) = 6000ml/minute.
The Dead Space: Is the space where no gas exchange occurs. It is either
anatomically (150 ml) (anatomical dead space nose, pharynx, larynx, trachea,
bronchi, bronchioles); or physiological dead space whereby some alveoli are not
functional because of absent or partial blood supply (normally it should be zero). So
the total dead space is the sum of anatomical and physiological dead spaces and so
equals to 150 ml. So the alveolar ventilation per minute equals to pulmonary
ventilation per minute minus dead space and equals to 500-150 = 350 ml/min X 12 =
4200 ml/min.
Respiratory passages: Nose trachea bronchi terminal bronchioles (all
contain cilia and mucus), then respiratory bronchioles alveolar sacs alveoli
(contain mucus).
9
Respiratory Physiology
Prof. Zaid Al-Madfai
Nerve stimulation (sympathetic, i.e., adrenalin dilatation; parasympathetic, i.e.,
Ach. constriction).
Cough reflex: afferent vagus nerve medulla autonomic inspiration of 2.5
liters closure of epiglottis and vocal cords contraction of abdominal muscles
sudden opening expel air at a velocity of 400 miles per hour + narrowing of
trachea and bronchi.
10
Respiratory Physiology
Prof. Zaid Al-Madfai
Sneeze reflex: Similar except to nasal passages instead of lower airways. Afferent is
fifth cranial medulla similar but depression of uvula so that large amounts of air
pass through the nose.
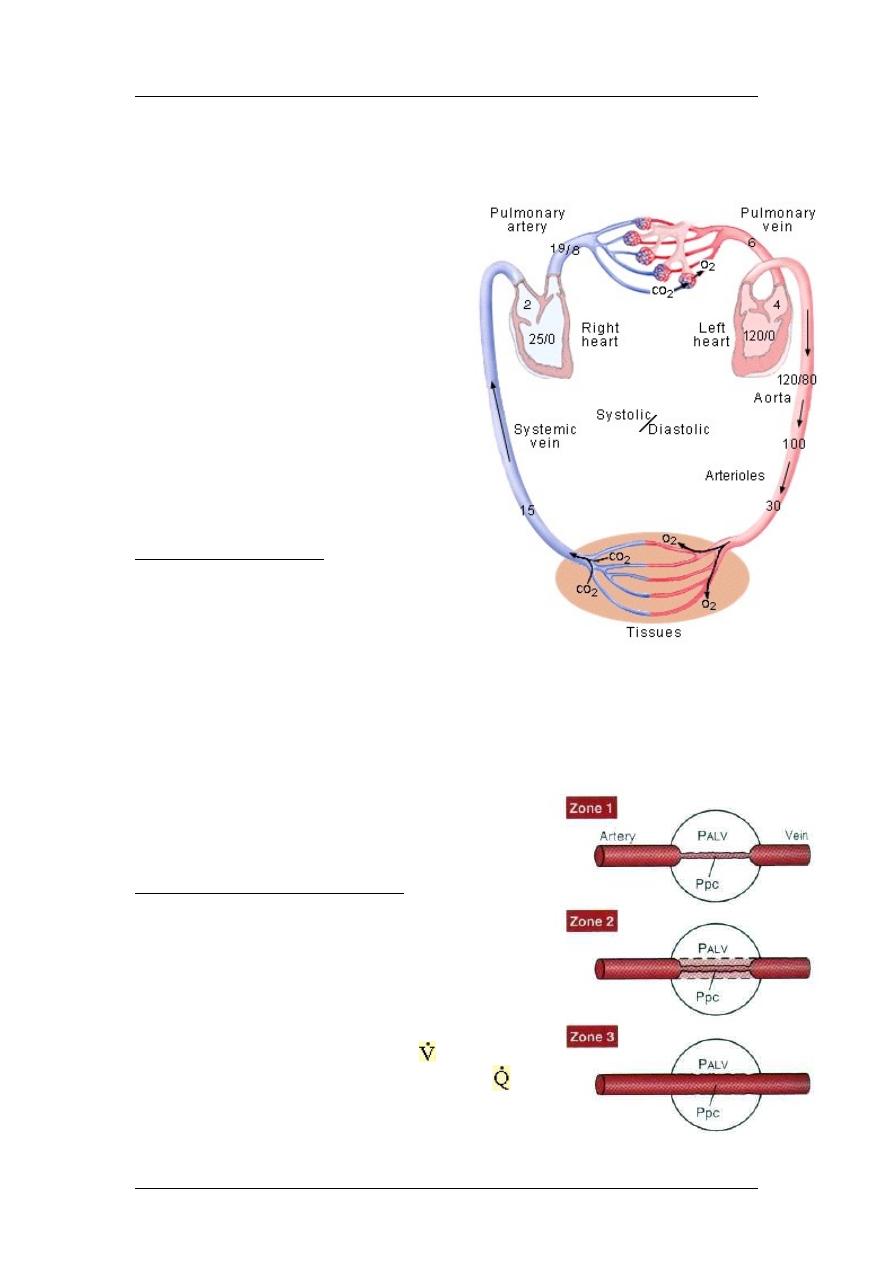
Pulmonary circulation
:
Blood supply to the lungs goes to bronchi
(nutrition) and respiratory units (gaseous
exchange).
When O2 concentration drops to 70%
(73mmHg), pulmonary blood vessels
constricts (opposite to other capillaries) and
this is important
shift the blood to more
aerated areas.
Right atrial pressure is 25 mmHg systolic
and 0 mmHg diastolic.
Pulmonary artery pressure is 25mmHg
systolic and 8mmHg diastolic (mean arterial
pressure equals 15 mmHg).
Pressures in the Lung
Various lung intravascular and
extravascular pressures influence
pulmonary blood flow and its
distribution in the lung. Pressure in different vascular segments (arteries,
capillaries and veins), extravascular pressures (intrathoracic or intrapleural),
and transmural pressure can vary considerably during both the cardiac and
respiratory cycles. Because these pressures can influence the distribution of
blood flow and vascular resistance, they can affect how well blood flow is
matched to ventilation.
Lung zones (1, no blood flow; 2, intermittent; 3,
always).
Ventilation-Perfusion Matching
The adult lung has about 300 million alveoli.
Each alveolus is surrounded by a capillary
mesh. Gas exchange is optimal in alveoli
where ventilation is closely matched to blood
flow or perfusion. More specifically, gas
exchange is optimal in alveoli where the
fraction of alveolar ventilation ( A) is
matched to the fraction of cardiac output ( )
11
Respiratory Physiology
Prof. Zaid Al-Madfai
perfusing that alveolus. For the whole lung, an ideal ventilation to perfusion
ratio ( A/ ) is between 0.8 to 1.0.
However, with 300 million alveoli, it is unlikely that ventilation will be
precisely matched to perfusion in each alveolus. Some alveoli may be
overventilated relative to their blood flow and exhibit a A/ > 1.0. Other
alveoli may be overperfused relative to their ventilation and have a A/ of
less than 0.8. At the extremes, some alveoli may be ventilated put receive no
perfusion (infinite A/ ), whereas other alveoli may be perfused but not
ventilated (very low A/ ). Normally in the upright lung, the A/ varies
slightly from the apex to the base of the lung because of disparities in the
distribution of ventilation and blood flow to these regions.
In the normal, upright adult, the lowest point in the lungs is about 30 centimeters
below the highest point. This represents a 23 mm Hg pressure difference, about 15
mm Hg of which is above the heart and 8 below.
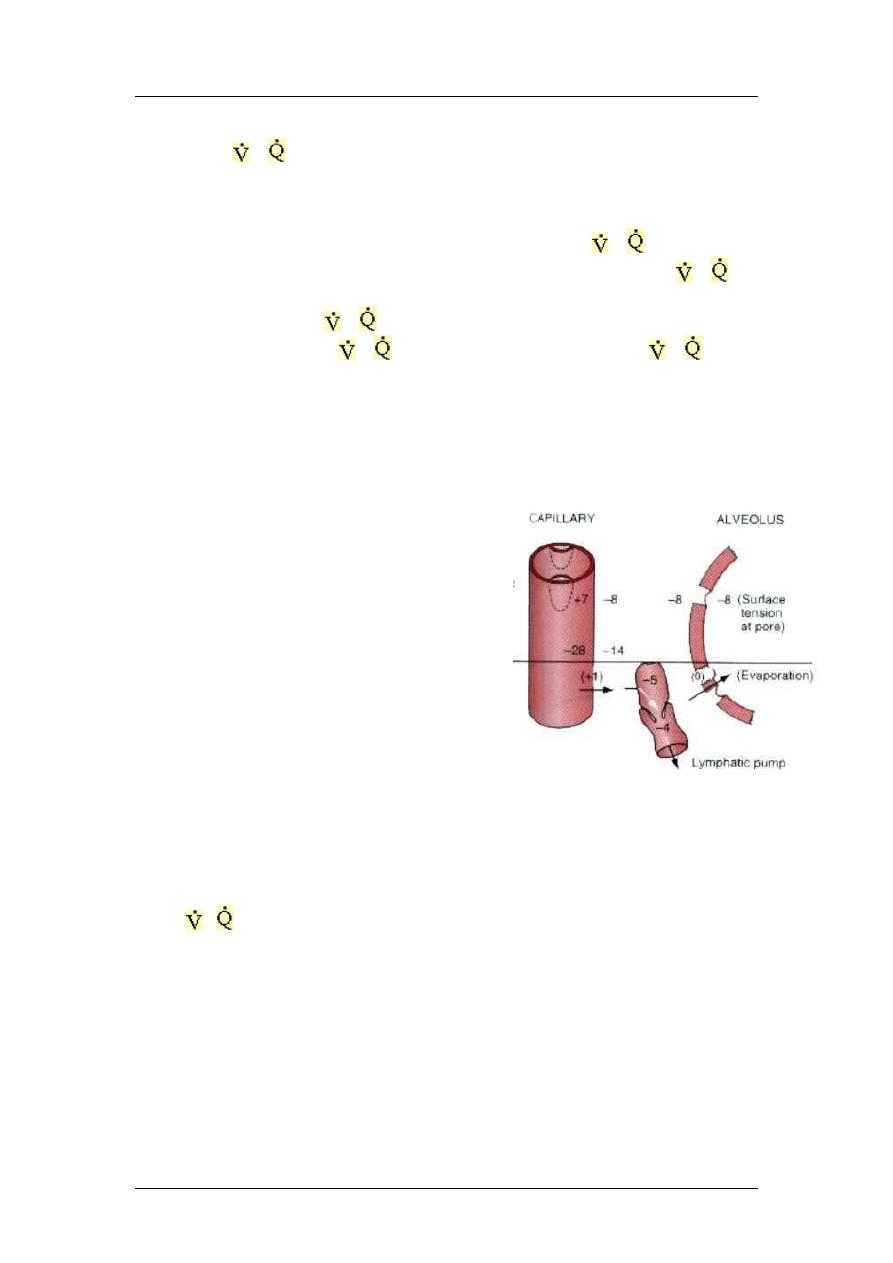
Perfusion across capillaries:
Capillary pressure equals 7mmHg (while it is 17
in general circulation).
Plasma colloid equals 28 mmHg.
Interstitial colloid 14 mmHg (7 in general
circulation)
-ve interstitial pressure equals 8 mmHg
Total = 29, so 29-28 = 1mmHg which removed by
lymphatics and evaporation
The pulmonary circulation receives the entire
output of the right heart, but vascular pressures
are considerably lower than in systemic vessels.
Lung vessels lack high resistance arterioles, which accounts for their low resistance to
blood flow. However, the lack of arterioles also compromises the ability of the lung to
readily control the distribution of blood flow. Blood flow in the upright lung is
distributed preferentially to the lung base because of the influence of gravity.
However, the base also receives a greater proportion of the ventilation than does the
apex. This imbalance in ventilation to perfusion in the upright lung can lead to a
higher
A
/ at the apex than the base. This is reflected by a higher alveolar PO
2
and
lower PCO
2
in alveoli at the apex than at lung base. Two types of edema, hydrostatic
and permeability, can occur in the lung. They have different etiologies and
characteristics and hence, require different therapeutic approaches. Hydrostatic edema
is related to increases in vascular pressure whereas permeability edema is caused by
an increased leakiness of lung capillaries to fluid and protein.
The blood volume of the lungs is about 450 milliliters, about 9 per cent of the total
blood volume of the entire circulatory system. Approximately 70 milliliters of this
pulmonary blood volume is in the pulmonary capillaries, and the remainder is divided
about equally between the pulmonary arteries and the veins.
12
Respiratory Physiology
Prof. Zaid Al-Madfai
Partial pressure of gases
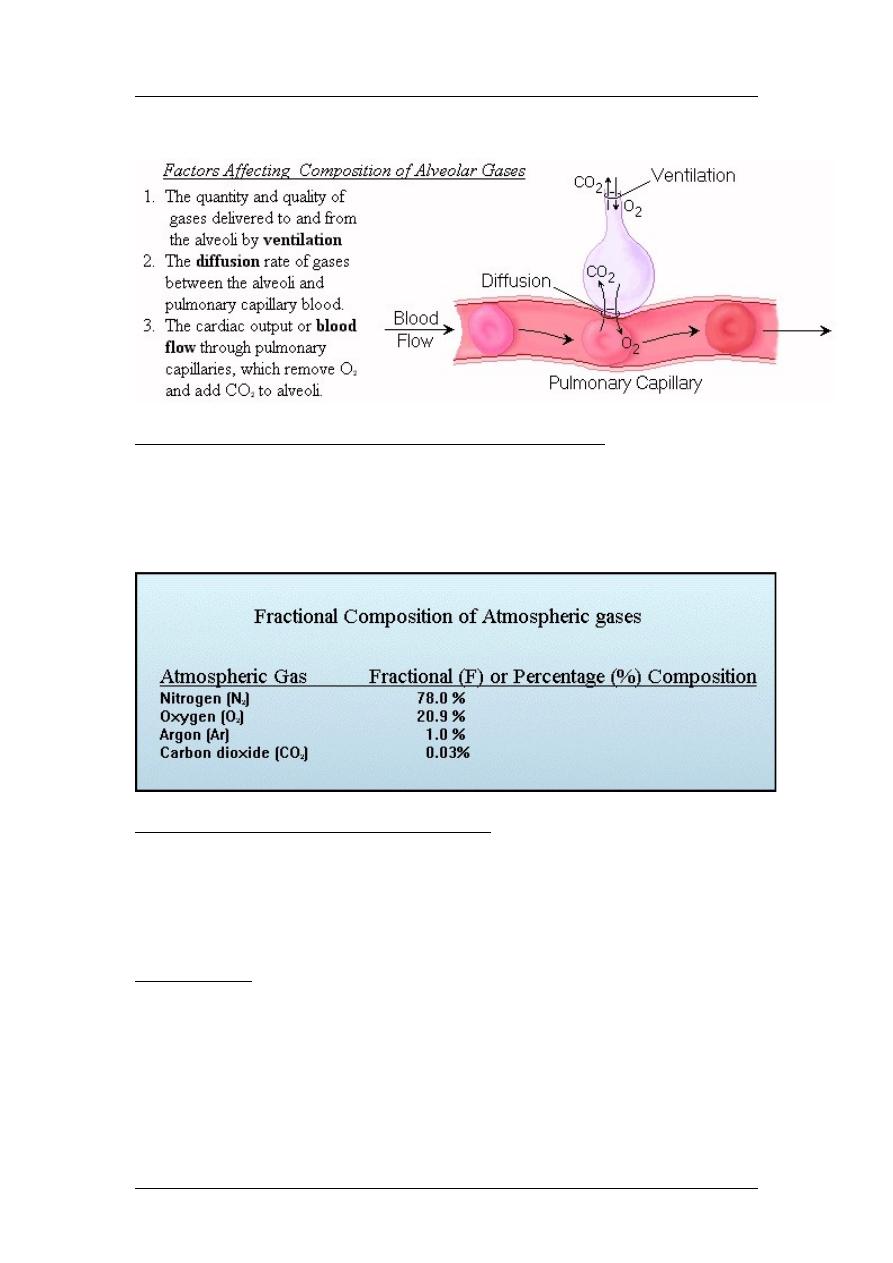
Ventilatory Factors Affecting Alveolar Gas Composition
The composition of alveolar gas depends on the amount and kind of gases
delivered to the alveoli by ventilation and on the rate of gas diffusion
between alveoli and pulmonary capillary blood. It also depends upon
pulmonary blood flow, which continuously delivers CO
2
and removes O
2
from
the alveoli.
Gases Comprising the Earth's Atmosphere
The earth's atmosphere is a mixture of gases consisting of about 78%
molecular nitrogen (N
2
), 20.9 % molecular oxygen (O
2
) and 1.0 % argon (Ar).
Other gases, like carbon dioxide (0.03%), are also detectable, but only in trace
amounts.
Dalton's Law
Dalton's Law states that the total pressure (i.e., barometric pressure; P
B
)
exerted by a mixture of gases, such as the earth's atmosphere, is equal to the
sum of the separate partial pressures each gas would exert if it occupied the
entire volume (space) alone. That is, the total pressure exerted by a mixture of
gases is equal to the sum of the individual partial pressures of the gases
comprising the mixture. For the earth's atmosphere, the total or barometric
pressure (P
B
) is the sum of the individual partial pressures of the gases
13

Respiratory Physiology
Prof. Zaid Al-Madfai
comprising the atmosphere. Thus, at a P
B
= 1 atmosphere (ATM) = 760, the
PN
2
= 594; PO
2
= 159; PAr = 7.1; and PCO
2
= 0.23.
Calculation of Partial Pressures for Atmospheric Gases
Clinically, it is often necessary to determine the partial pressure of a particular
gas in a gas mixture. The partial pressure (Pg) of a given gas (g) in a mixture
of gases is computed by multiplying total gas pressure by the fractional
concentration of the gas in the gas mixture. To simplify the calculation, the
fraction of O
2
present in ambient air is generally taken to be 0.21 or 21%.
Thus, at sea level, where total pressure or P
B
= 760 Torr, the partial pressure of
O
2
(PO
2
) is computed by multiplying P
B
by the fraction of O
2
in the gas
mixture. The fractional composition of air in Denver, Colorado is the same as
at sea level. However, the PO
2
in Denver, Colorado is less because it is 1 mile
above sea level and the P
B
of Denver averages about 625 Torr.
The Addition of Water Vapor to Inspired Air
Ambient air inhaled into the nasal passages and tracheobronchial tree is
immediately warmed to body temperature and completely saturated with
water vapor. The water vapor or water gas added to inspired air exerts a partial
pressure just like the other gases comprising air. The ability and capacity of air
to hold water vapor increases as the temperature of the air increases and is
independent of the total air pressure. At body temperature (37
o
C), air,
saturated with water vapor has a water vapor pressure (PH
2
O) of 47 Torr,
provided P
B
exceeds PH
2
O. In a more practical sense, the PH
2
O in the airway
of a person at sea level is the same as a person in Denver if their body
temperatures are the same. Like the other gases present in air, PH
2
O also
Law. As a consequence, the addition of water vapor to inspired
air reduces the partial pressure of other gases without changing the total gas
pressure. For air in the tracheobronchial tree, P
B
is the sum of the partial
pressure of atmospheric gases plus water vapor or P
B
= PN
2
+ PO
2
+PCO
2
+
PAr +PH
2
O + Pother gases.
14

Respiratory Physiology
Prof. Zaid Al-Madfai
Composition of gases in air:
Atm.
Atm. +
humidity
alveolar
Expired
N2
597.0
563.4
569.0
566.0
O2
159.0
149.3
104.0
120.0
CO2
0.3
0.3
40.0
27.0
H2O
3.7
47.0
47.0
47.0
Composition of Alveolar Gases
With normal diffusion, the composition of alveolar gases is largely determined
by two interacting processes.
1. Ventilation: the periodic partial replacement and dilution of alveolar air
with fresh ambient air during inspiration and the exhalation of a portion of
alveolar air during expiration.
2. Blood flow: blood traversing the pulmonary capillaries continuously
delivers CO
2
, produced by the tissues, to the alveoli for excretion, while
concurrently extracting O
2
from the alveoli for transport to the tissues.
Only a portion of each tidal volume is delivered to the alveoli. The total air
volume of all lung alveoli before inspiration (end-expiration) is by definition
the
. For a normal adult, the FRC is about 2500
ml. So, if the volume of fresh ambient air reaching the alveoli is 300 ml, it is
added to an FRC of 2500 ml. As a result, the partial pressures of alveolar
gases do not fluctuate markedly with each breath since only a portion of the
FRC is exchanged.
Factors affecting the diffusion of gasses in air:
∆
Pressure X Area X Temperature
D = ----------------------------------------------,
distance X SQR(Molecular Weight)
diff. coef. = T/SQR(MW)
(constant)
Factors affecting pressure of gas in fluid: concentration and solubility
Solubility of O2 = 0.024
Solubility of CO2 = 0.57 (20 times of O2)
Diffusion of gases through fluids depends on several factors:
1) solubility, 2) cross section, 3) distance, 4) MW, 5) solubility
∆
Pressure X Area X Solubility
D = ----------------------------------------------,
distance X SQR(Molecular Weight)
diff. coef. = S/SQR(MW)
(constant)
∆
P X A
So D = --------- X diff. coef.
d
15
Respiratory Physiology
Prof. Zaid Al-Madfai
If the diff. coef. of O2 is (1), then the relative coef of CO2 is (20.3), CO is (0.81), N2
is (0.53)
Diffusion of gases through tissues: all gases concerned are highly soluble in lipids, so
in tissues, all factors affecting diffusion in water is the same.
Rate of exchange of gases in alveoli: residual capacity = 2300, while only 350 ml
enters (1/7), so many breaths are needed to fully change the alveolar air, which is
important to prevent sudden changes in respiratory control center.
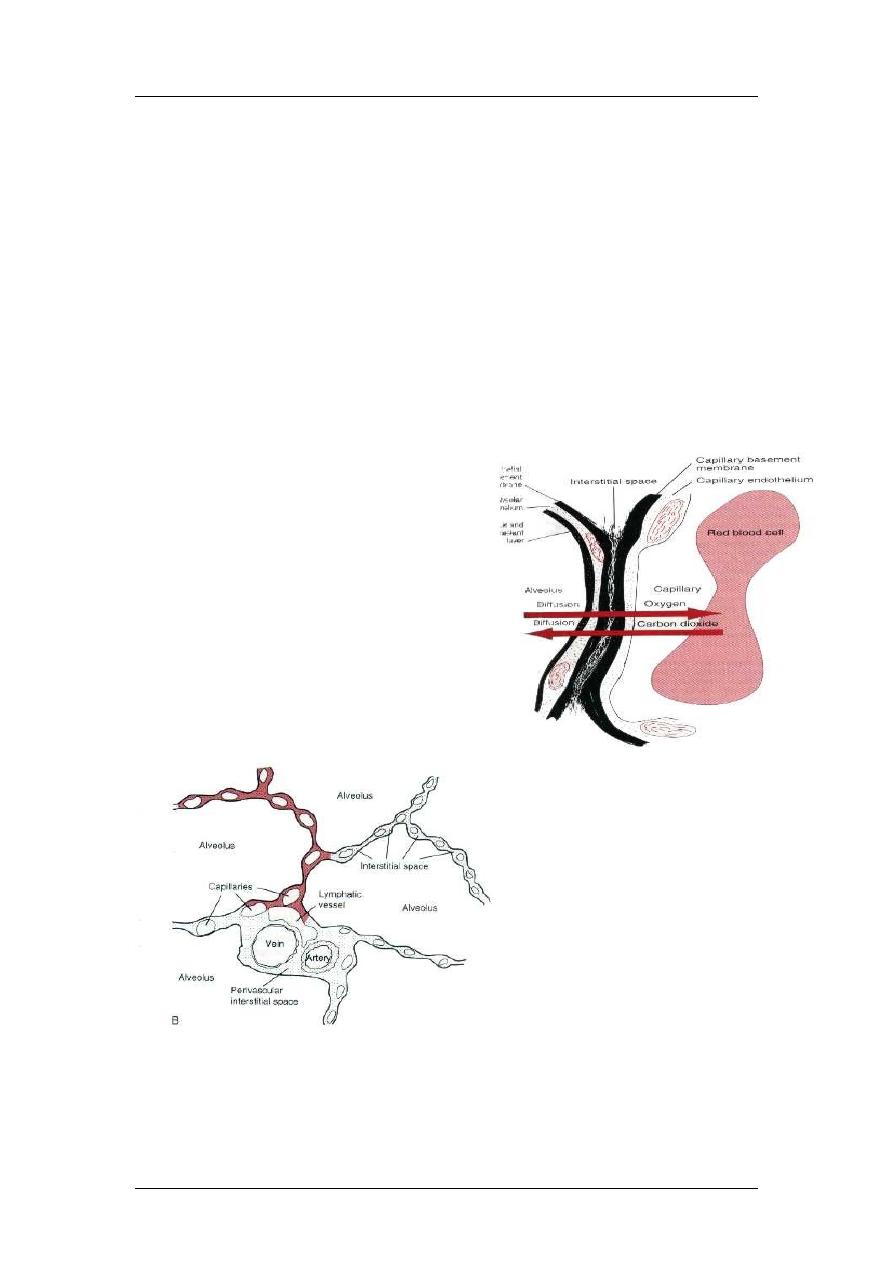
Diffusion of Gases through the Respiratory Membrane
The respiratory unit: respiratory bronchioles, alveolar ducts, atria, and alveoli.
Blood flows as a sheet.
Respiratory membrane is 0.2 micrometer thickness and composed of: 1) fluid
(surfactant), 2) epithelium, 3) epithelial basement membrane, 4) interstitial fluid, 5)
capillary basement membrane, 6) endothelial cells.
The total surface area is 70 m
2
and contain 60-140ml blood. The diameter of the
capillary is 5micrometers (RBC is 7 micrometers), so RBC squeeze inside.
16

Respiratory Physiology
Prof. Zaid Al-Madfai
Respiratory membrane diffusion capacity
= volume of gas diffusing
through membrane / minute for pressure difference of 1 mmHg.
The mean oxygen pressure difference across the respiratory membrane during normal,
quiet breathing is about 11 mm Hg. Multiplication of this pressure by the diffusing
capacity (11 × 21) gives a total of about 230 milliliters of oxygen diffusing through
the respiratory membrane each minute; this is equal to the rate at which the resting
body uses oxygen. In exercise, diffusion capacity increases to 65 because of (1)
opening of dormant capillaries and (2) better ventilation perfusion ratio.
Diffusion capacity for CO2 = 400-450 ml/min/mmHg and in exercise increases to
1200-1300.
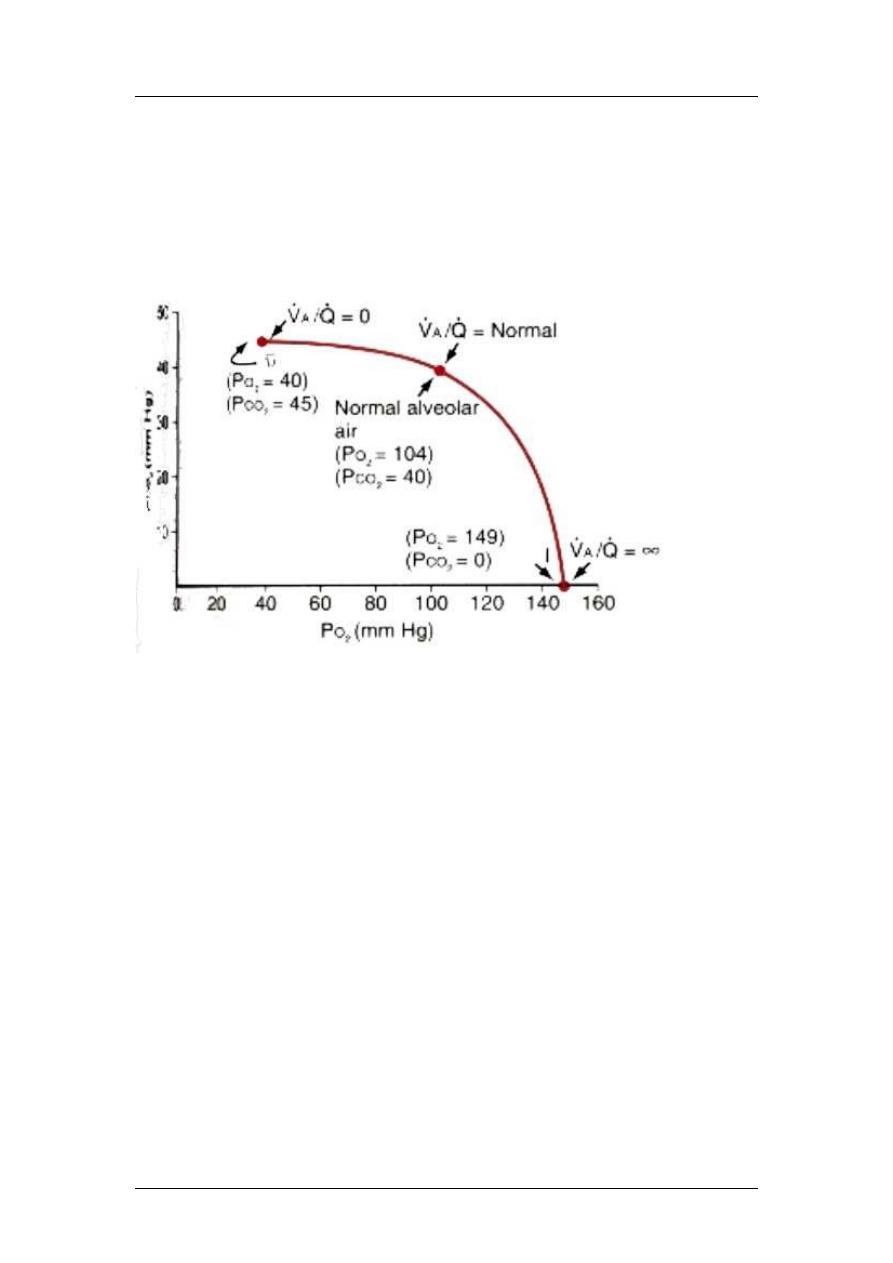
Effect of ventilation perfusion ratio on alveolar gas
concentration:
Ventilation-perfusion ratio (ranges from 0 to infinity):
- Alveolar Oxygen and Carbon Dioxide Partial Pressures when VA/Q Equals Zero,
that is, without any alveolar ventilation-the air in the alveolus comes to equilibrium
with the blood oxygen and carbon dioxide because these gases diffuse between the
blood and the alveolar air. Because the blood that perfuses the capillaries is venous
blood returning to the lungs from the systemic circulation, it is the gases in this blood
with which the alveolar gases equilibrate. The normal venous blood has a PO2 of 40
mm Hg and a PCO2 of 45 mm Hg. Therefore, these are also the normal partial
pressures of these two gases in alveoli that have blood flow but no ventilation.
- Alveolar Oxygen and Carbon Dioxide Partial Pressures when VA/Q Equals Infinity,
there is no capillary blood flow to carry oxygen away or to bring carbon dioxide to the
alveoli. Therefore, instead of the alveolar gases coming to equilibrium with the
venous blood, the alveolar air becomes equal to the humidified inspired air. That is,
the air that is inspired loses no oxygen to the blood and gains no carbon dioxide from
the blood. And because normal inspired and humidified air has a PO2 of 149 mm Hg
and a PCO2 of 0 mm Hg, these will be the partial pressures of these two gases in the
alveoli.
- Gas Exchange and Alveolar Partial Pressures when VA/Q Is Normal, when there is
both normal alveolar ventilation and normal alveolar capillary blood flow (normal
alveolar perfusion), exchange of oxygen and carbon dioxide through the respiratory
membrane is nearly optimal, and alveolar PO2 is normally at a level of 104 mm Hg,
which lies between that of the inspired air (149 mm Hg) and that of venous blood (40
mm Hg). Likewise, alveolar PCO2 lies between two extremes; it is normally 40 mm
Hg, in contrast to 45 mm Hg in venous blood and 0 mm Hg in inspired air. Thus,
under normal conditions, the alveolar air Po2 averages 104 mm Hg and the Pco2
averages 40 mm Hg.
VA/Q = 0 O2 = 40, CO2 = 45mmHg
VA/Q = infinity O2 = 149, CO2 = 0mmHg
VA/Q = normal O2 = 104, CO2 = 40mmHg
If less than normal then called physiological shunt
If more than normal then called physiological dead space
17
Respiratory Physiology
Prof. Zaid Al-Madfai
Normally at the tip of the lung, VA/Q is (2.5) times normal (phys. dead space), while
at the base, it is (0.6) times normal (phys. shunt).
Normally, there are abnormal VA/Q ratios in the upper and lower portions of the lung.
In the upper both ventilation and perfusion are low but VA is more than Q, so there is
physiological dead space, but in the lower VA is less than Q, so there is physiological
shunt.
Abnormally, as in smokers, bronchi obstruction emphysema (1) low ratio [no
air] and (2) high ratio because of obstructed alveolar wall.
Transport of O2 and CO2
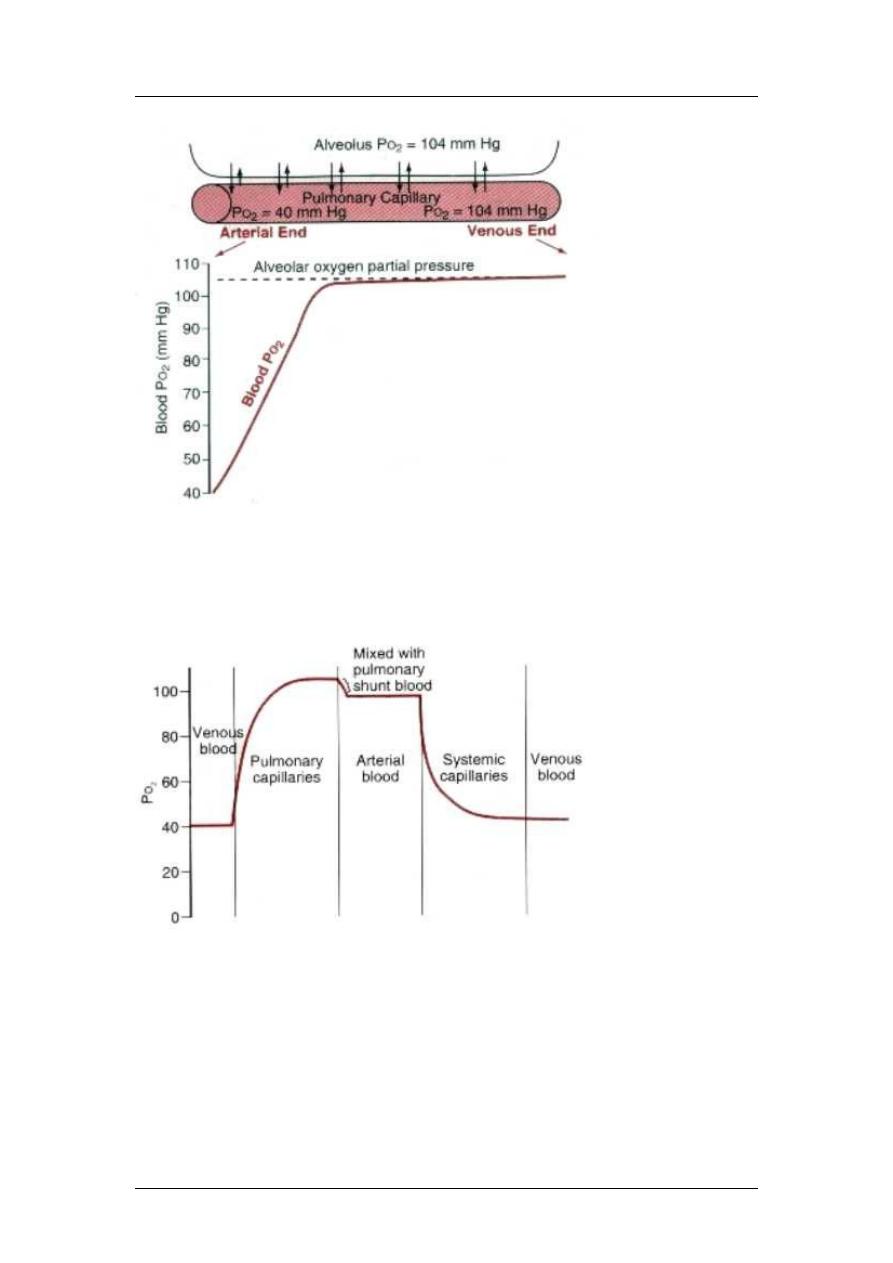
Blood in capillaries become fully saturated (40 104mmHg) in the first 1/3 of
capillary passage in alveolus. In exercise, there is 20 fold increase demand for O2 but
as the diffusion capacity is increased 3 folds, opening of other capillaries leading to
better VA/Q ratio and the last 2/3 of the capillary length.
18
Respiratory Physiology
Prof. Zaid Al-Madfai
98% of blood become saturated with O2 and the rest (2%) is shunted (bronchial
circulation), so ending in pulmonary vein O2 saturation of 95mmHg (not 104).
This blood (95mmHg) diffuse to the interstitial space (40mmHg) then to cells
(23mmHg).
For CO2, intracellular (46mmHg) interstitial space (45mmHg) veins (45mmHg)
alveoli (40mmHg).
Transport of O2 in blood:
97% of O2 in blood is transported by combining with hemoglobin and only 3% is
dissolved.
O2 + Hb HbO2
19
Respiratory Physiology
Prof. Zaid Al-Madfai
Partial pressure of blood leaving the lung is 95mmHg = 97% saturation and venous
blood contains 40mmHg (75% saturation).
Each gram of Hb binds to 1.34ml O2, so 1.34 X 15gm = 20.1ml O2 in 100%
saturation. So 95mmHg (97%) blood carries 19.4ml O2 tissues (40% saturation)
veins (70%) carrying 14.4mlO2.
All this is in the resting state, in exercise, PO2 in tissues is low to 15mmHg, where
more O2 is delivered leaving blood with only 4.4ml O2.
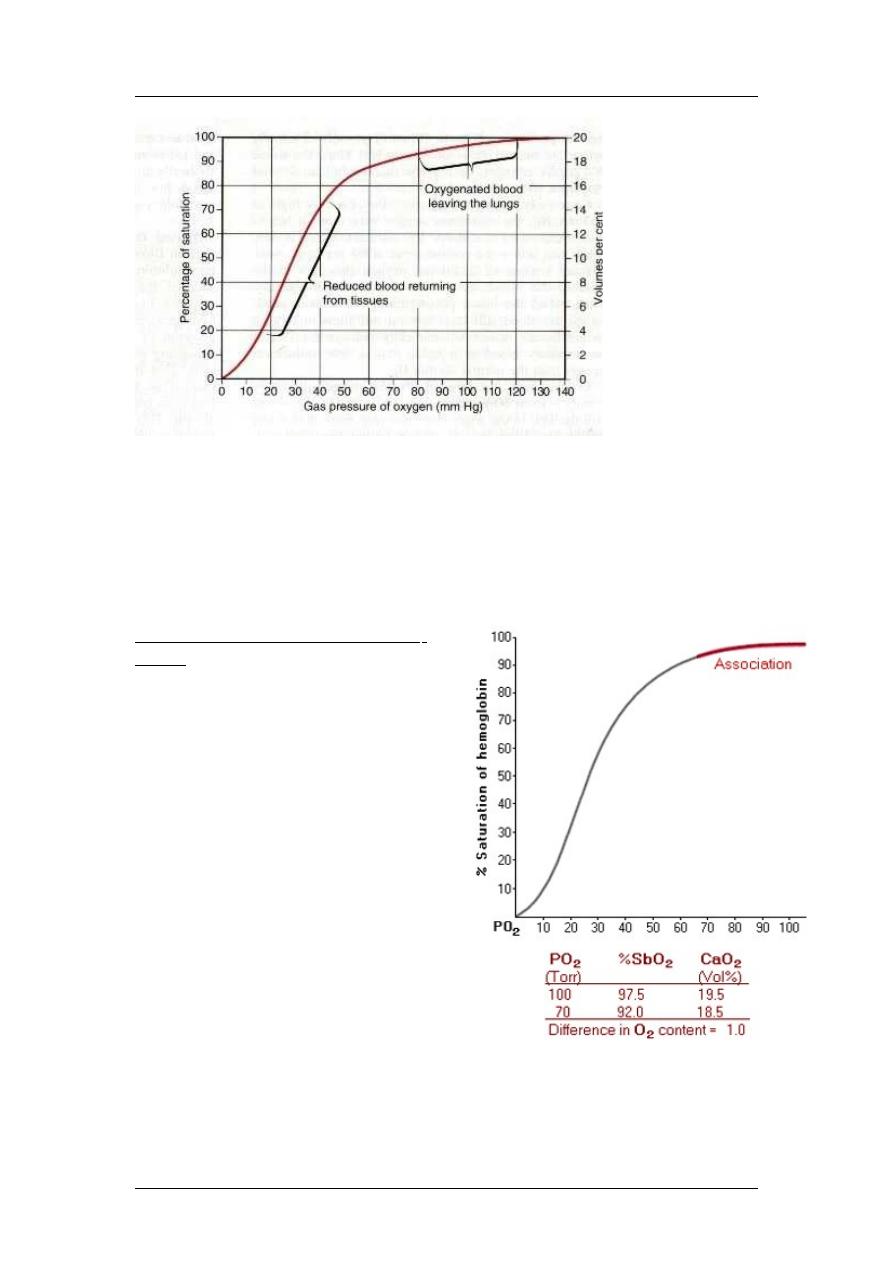
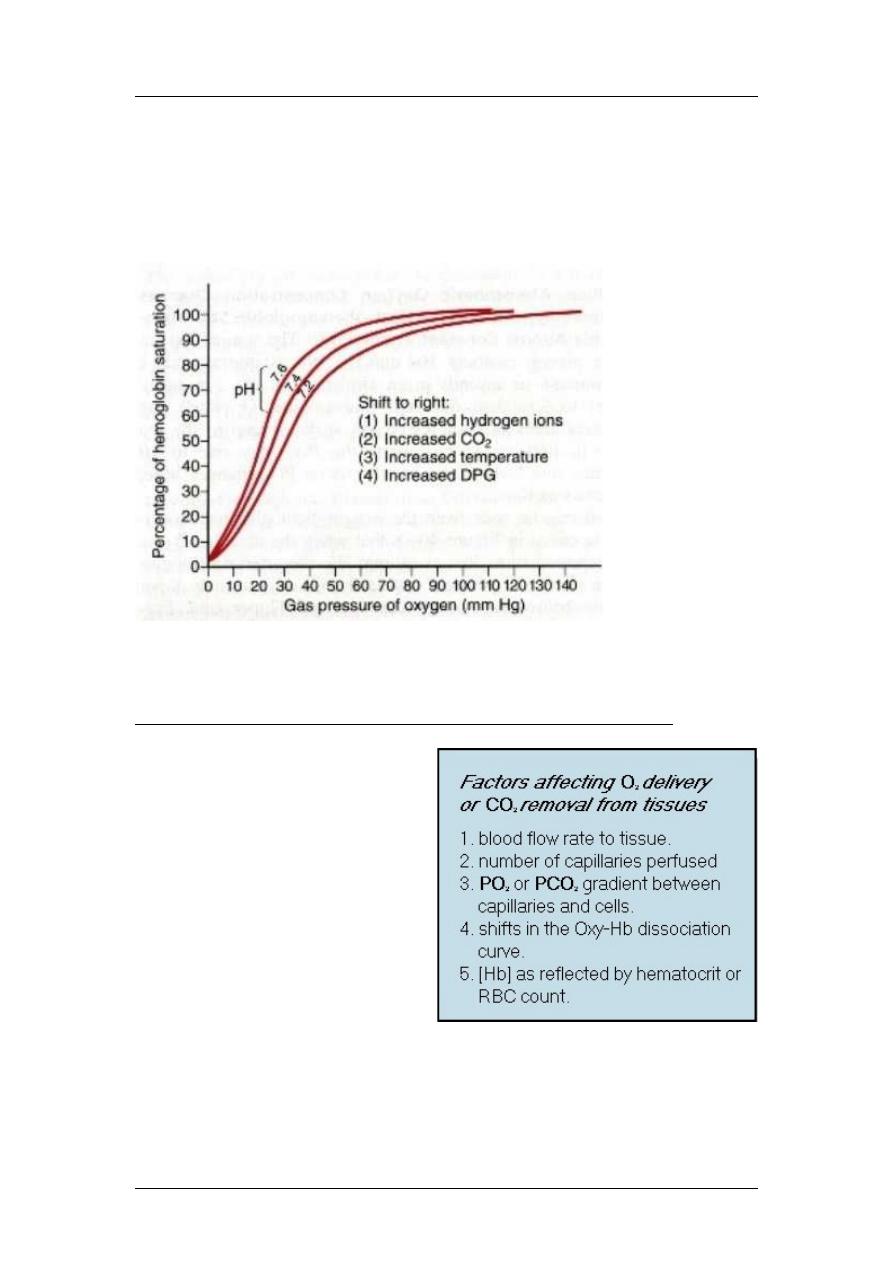
Shape of the Oxy-Hb Dissociation
Curve
The sigmoidal shape of the oxy-Hb
dissociation curve has physiological
importance for both the loading of
O
2
in the lungs and for unloading O
2
in the tissue capillaries. The upper
portion of the curve, between a PO
2
of 70 to 100 Torr, is nearly flat. This
portion of the curve is often referred
to as the association part of the curve
because it is important in the loading
of O
2
(association of O
2
with Hb) in
the lung capillary. The association
part of the curve insures oxygenation
of most of the Hb even when
alveolar PO
2
is decreased due to
altitude ascension or pulmonary
disease. The SbO
2
decreases from
97.5% at a PO
2
of 100 Torr to 92%
at a PO
2
of 70 Torr with only a change of 1.0 vol% in blood O
2
content. Thus,
this flat portion of the oxy-Hb dissociation curve insures nearly normal
loading of Hb with O
2
even when the alveolar PO
2
is reduced from normal.
20
Respiratory Physiology
Prof. Zaid Al-Madfai
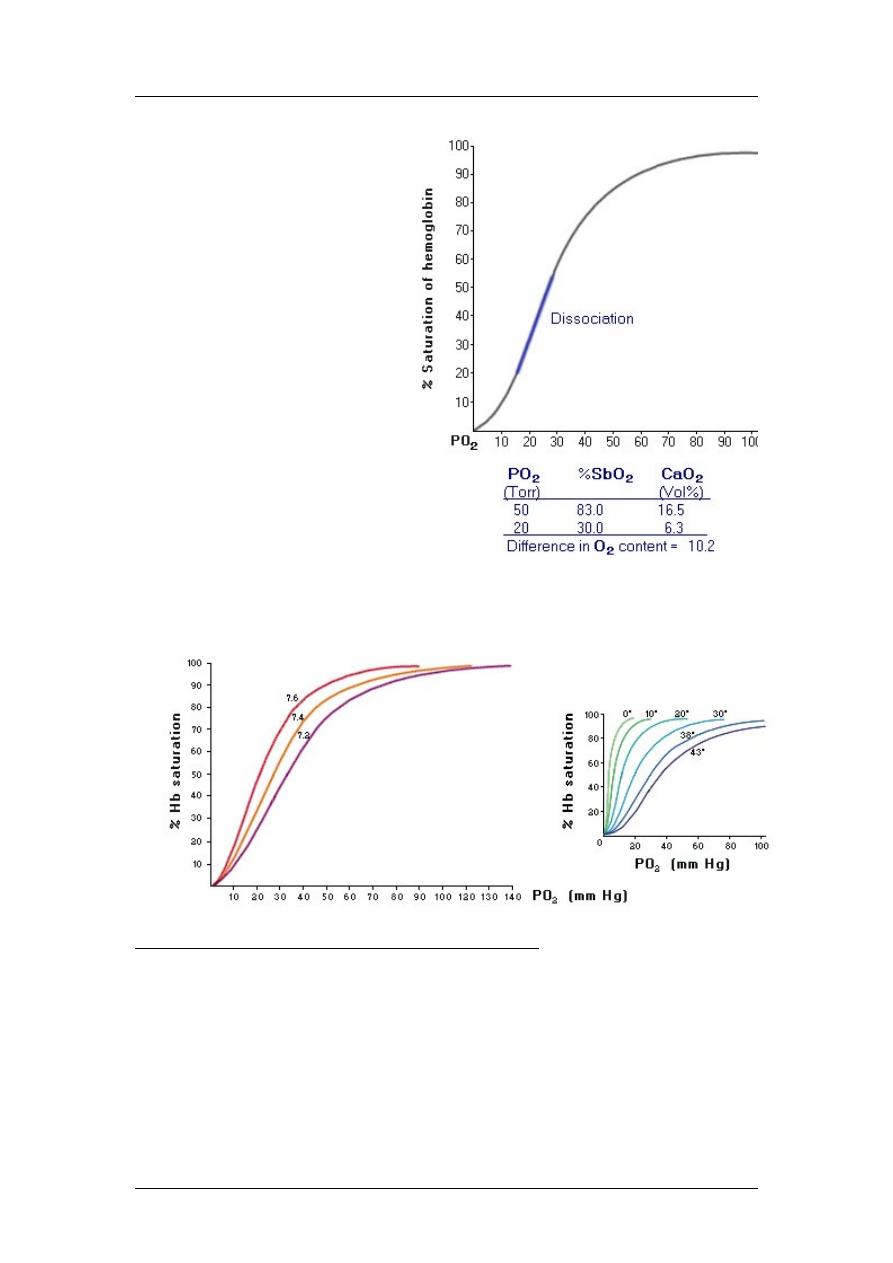
On the other hand, the steep
sloping part of the curve,
between a PO
2
of 50 and 20
Torr is termed the
dissociation portion of the
curve. The dissociation
portion of the curve is
important in the tissue
capillaries where a large
amount of O
2
can be unloaded
for a relatively small change
in the PO
2
. For example, a
decrease in the PO
2
from 50
to 20 Torr reduces the blood
O
2
content by over 10 vol% or
by nearly 50%. Thus, a
sizable portion of the O
2
carried by Hb is available for
use by the tissues for a
relatively small change in the
PO
2
. In other words, Hb relinquishes a relatively large amount of O
2
for a
small change in the PO
2
. The transition from the association to dissociation
portion of the curve is normally at a PO
2
of around 60 Torr. The curve is very
steep below, and relatively flat above this PO
2
Shifts in the Oxyhemoglobin Dissociation Curve
The oxy-Hb dissociation curve is also capable of shifting to the right or to the
left. An increase in the blood PCO
2
or hydrogen ion concentration [H
+
]
(decrease pH) shifts the curve to the right, whereas a decrease in PCO
2
or [H
+
]
(increase pH) shifts the curve to the left. Shifts in the oxy-Hb dissociation
curve due to changes in the blood PCO
2
or pH are termed the Bohr effect. An
increase in blood temperature or 2,3-diphosphoglycerate (2,3-DPG) levels in
the RBC also shift the oxy-Hb dissociation curve to the right, while a decrease
in temperature or 2,3-DPG shifts the curve to the left. A shift in the oxy-Hb
21
Respiratory Physiology
Prof. Zaid Al-Madfai
dissociation curve to the right means that more O
2
is liberated for a given
decrease in the PO
2
. Stated another way, a shift in the curve to the right
indicates that the affinity of Hb for O
2
is reduced, so that for a given plasma
PO
2
, more O
2
is freed from Hb. In contrast, a shift in the curve to the left
means more O
2
will be attached to Hb (increased affinity) for a given PO
2
.
Thus, less O
2
is available to the tissues or is freed from Hb at a given PO
2
.
Bohr effect: in the lungs, removal of CO2 from blood shift to the left more O2
binding, while in tissues, increase CO2 in blood shift to the right easy release of
O2.
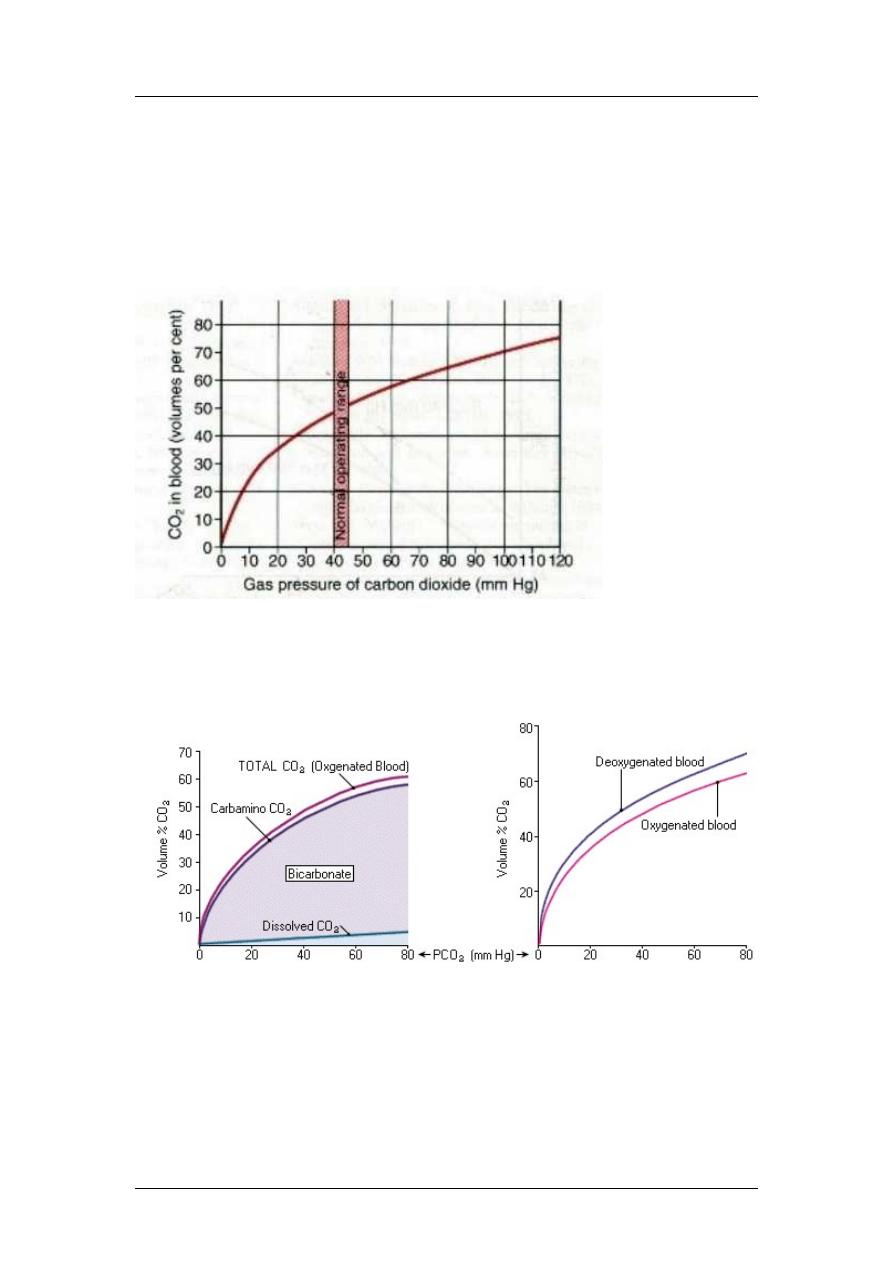
Factors Affecting O
2
Delivery an CO
2
Removal from the Tissues
Blood flow rate is the primary
factor that affects O
2
delivery to
the tissues. An increase in blood
flow typically results in an
equivalent increase in O
2
delivery. Increasing the number
of open capillaries is another
way to increase O
2
delivery to a
tissue. An increase in the partial
pressure gradient between the
capillary and tissue also
enhances O
2
delivery. Shifts in
the oxy-Hb dissociation curve
related to changes in the acid-
base characteristics of the blood can also alter O
2
delivery to tissues. Likewise,
an increase in the number of RBCs or hematocrit (i.e., [Hb]) also increases the
amount of O
2
delivered to the tissues. Many of the above factors that increase
O
2
delivery also facilitate CO
2
removal.
22
Respiratory Physiology
Prof. Zaid Al-Madfai
Transport of CO2 in blood
Under normal conditions, 4ml of CO2/100ml blood.
CO2 leaves the cell interstitial fluid blood in dissolved state. Inside the
capillary, it is either dissolved (7%), or as bicarbonates (depends on carbonic
anhydrase which increase the reaction to 5000 times, this enzyme is found in RBCs),
where bicarbonates diffuse outside the RBC and chloride is shifted inside
(bicarbonate-chloride shift carrier protein) and hydrogen ion is buffered by Hb (70%),
and the rest is carried as carbaminohemoglobin compound (23%).
Haldane effect: opposite to Bohr effect, when O
2
binds to Hb CO
2
is released,
which is more important for the transport of CO
2
than O
2
. In other words, when Hb
loses O
2
, it becomes a stronger base or weaker acid, making more sites available to
buffer H
+
. When O
2
combine with hemoglobin in the lungs acid Hb less
combination with CO
2
to form carbaminohemoglobin and also acid Hb release of
H
+
which combines with HCO3
-
H
2
CO
3
CO
2
+ H
2
O.
23
Respiratory Physiology
Prof. Zaid Al-Madfai
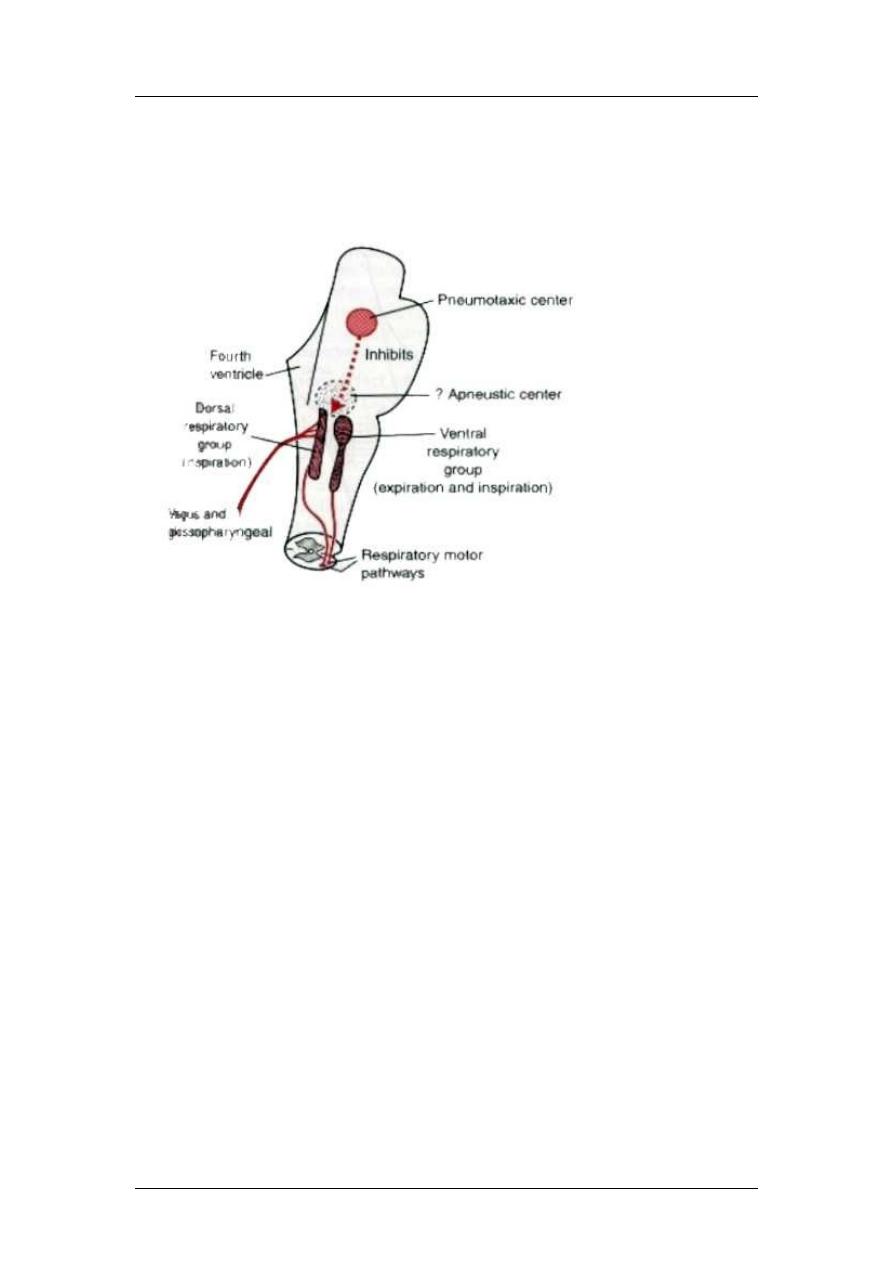
Regulation of respiration
1- Dorsal group (inspiration)
2- Ventral group (expiration and inspiration)
3- Pneumotaxic center (rate and pattern)
4- Apneustic center
Dorsal group (located in the medulla) receive from the vagus (peripheral
chemoreceptors, baroreceptors and lung receptors). They are responsible for the
rhythm (unknown cause). Normal inspiration.
Ventral group: Located at the medulla, they remain inactive during quite breathing
but on increase need, signals from the dorsal to ventral contribution of ventral to
respiration. They cause inspiration and expiration. Active expiration.
Pneumotaxic center: Located at the upper one-third of the pons, it sends signals to
the inspiratory center to switch off inspiratory ramp. When the pneumotaxic signal is
strong, inspiration is terminated in 0.5 seconds, but when weak, then termination
occurs after 5 seconds. So this center can affect the rate of respiration.
Apneuostic center: Located at the lower two-thirds of the pons, may send signals to
the dorsal to prevent or retard the switch off of the respiratory ramp lung filled
with air.
Lung inflation signals:
The Hering-Breuer Inflation reflex (also called inhibito-inspiratory reflex) is initiated
by stretch receptors (sensors) located in the smooth muscles surrounding both large
and small airways. With lung inflation, these stretch receptors are stimulated and send
neural signals via vagal afferents that appear to be inhibitory to the pontine apneustic
center. Thus, they function to facilitate termination of inspiration. There is also a
Hering-Breuer Deflation reflex (or excito-inspiratory reflex). This reflex is initiated
either by decreased activity in the same airway stretch receptors involved in the
inflation reflex or by stimulation of other proprioceptors that are activated by lung
deflation. This information is also conveyed via vagal afferents to the brain stem
respiratory centers to encourage inspiration. While Hering-Breuer reflexes are readily
demonstrated in anesthetized animals, they are more difficult to demonstrate in
24
Respiratory Physiology
Prof. Zaid Al-Madfai
humans, except at large tidal volumes. These reflexes are detectable in infants and are
probably important in regulating the work of breathing.
In humans, this reflex is activated when the tidal volume is more than 1.5 liters, so it
is a protective reflex.
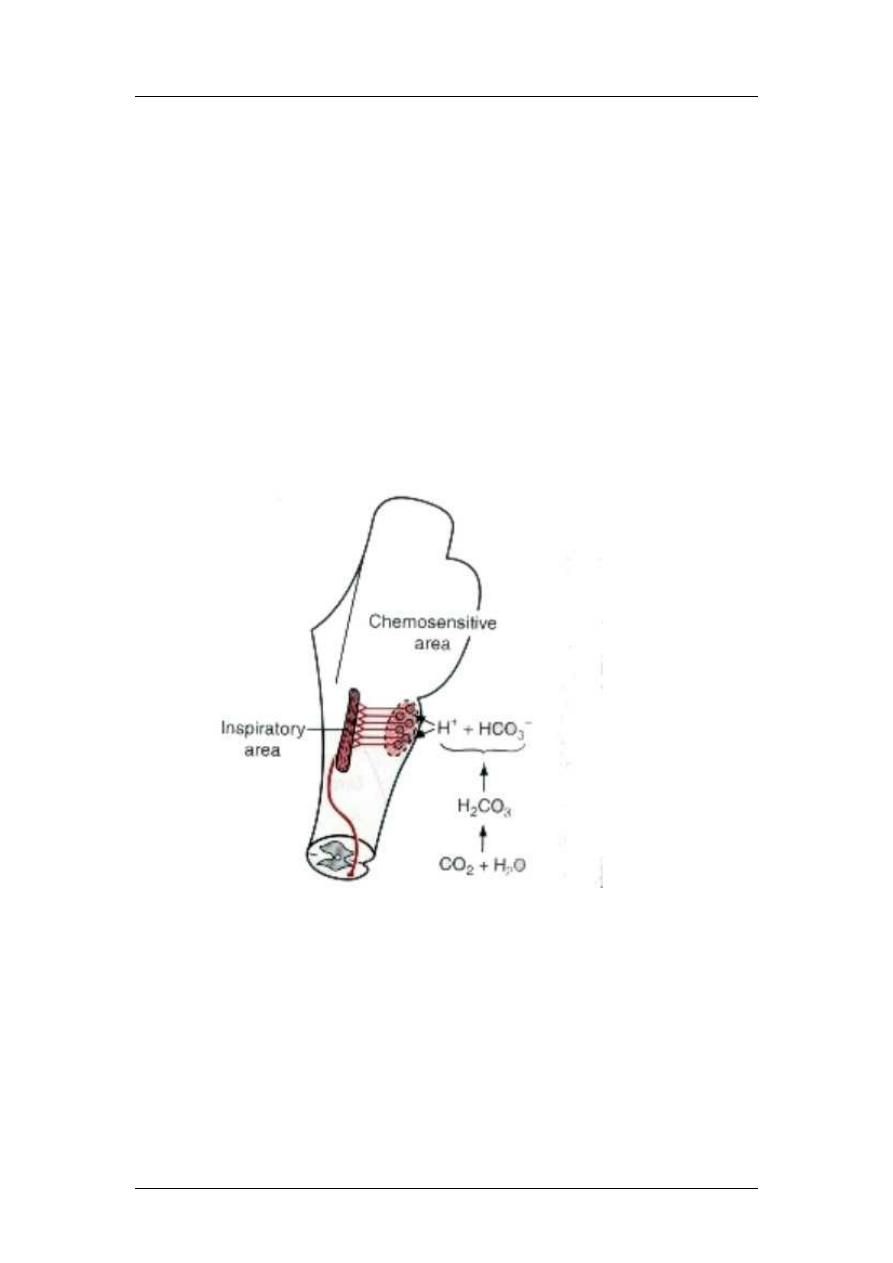
Chemical control of respiration
The chemoreceptors are specialized cells capable of detecting changes in the
concentration of physically dissolved O
2
, CO
2
, or hydrogen ion (H
+
) in the
extracellular fluid immediately surrounding them. These chemosensitive cells are
divided functionally, anatomically and geographically into the peripheral and central
chemoreceptors. They function to regulate ventilation so CO
2
is maintained nearly
constant and at a level consistent with CO
2
production and O
2
consumption by the
tissues of the body.
In the central chemoreceptors, CO2 and H
+
effect: H
+
are the most potent stimulator,
but they does not cross the blood brain barrier, but when CO
2
increases, it passes the
BBB and so it forms H
+
to stimulate the chemosensitive area in the medulla near the
respiratory center.
It has a very acute effect (in hours), but after 1-2 days, it decreases because of renal
HCO
3
-
formation.
The peripheral chemoreceptors are located in discrete structures known as the carotid
and aortic bodies.
O
2
has no direct effect but through peripheral chemoreceptors (aortic and carotid
bodies). They have little effect compared to CO
2
and H
+
. The carotid send impulses
through Hering's nerve glossopharangeal nerve to dorsal group. Aortic vagus
dorsal group.
These receptors (aortic and carotid bodies) are sensitive to O
2
(30-60mmHg). They
are also sensitive to CO
2
and H
+
but the effect of CO
2
and H
+
on the respiratory center
is stronger than on the chemoreceptors.
25

Respiratory Physiology
Prof. Zaid Al-Madfai
Acclimatization: mountain climbers, after 1-2 days, the CO2 effect will be lost and
O2 will increase ventilation to 400-500%.
In exercise, increase ventilation is due to (1) motor stimulation of muscles spread to
respiratory center, (2) joint movement also.
Other factors controlling respiration:
1- Voluntary control
2- Pulmonary irritant receptors
3- Lung j-receptors (at the junction of alveoli to capillaries). The Pulmonary J-
receptors, an abbreviated name for the pulmonary juxtapulmonary-capillary
receptors, are located in, or near, the walls of pulmonary microvessels. They
appear to be stimulated by vascular emboli, interstitial edema, and certain
chemicals (phenyldiguanide or capsaicin). Information from the J-receptors is
also delivered via vagal afferents to the brain stem. Their stimulation results in
rapid shallow breathing (tachypnea). These receptors are thought to be
responsible for the psychological sensation of "air hunger", also known as
dyspnea. Dyspnea is characterized by the sensation of labored breathing and
"shortness" of breath.
Periodic breathing: deep and shallow, for example:
Chyne-Stokes breathing: on fast breathing, CO2 is decreased and O2 is increased
respiratory depression and after few seconds, it recurs. It is found in all normal
subjects but damped by the fluids of blood, and the brain contains dissolved CO2 and
O2 to minimize the effect but it can occur in:
1- Severe heart failure, where slow blood circulation to the brain
2- Brain damage reverse feed-back
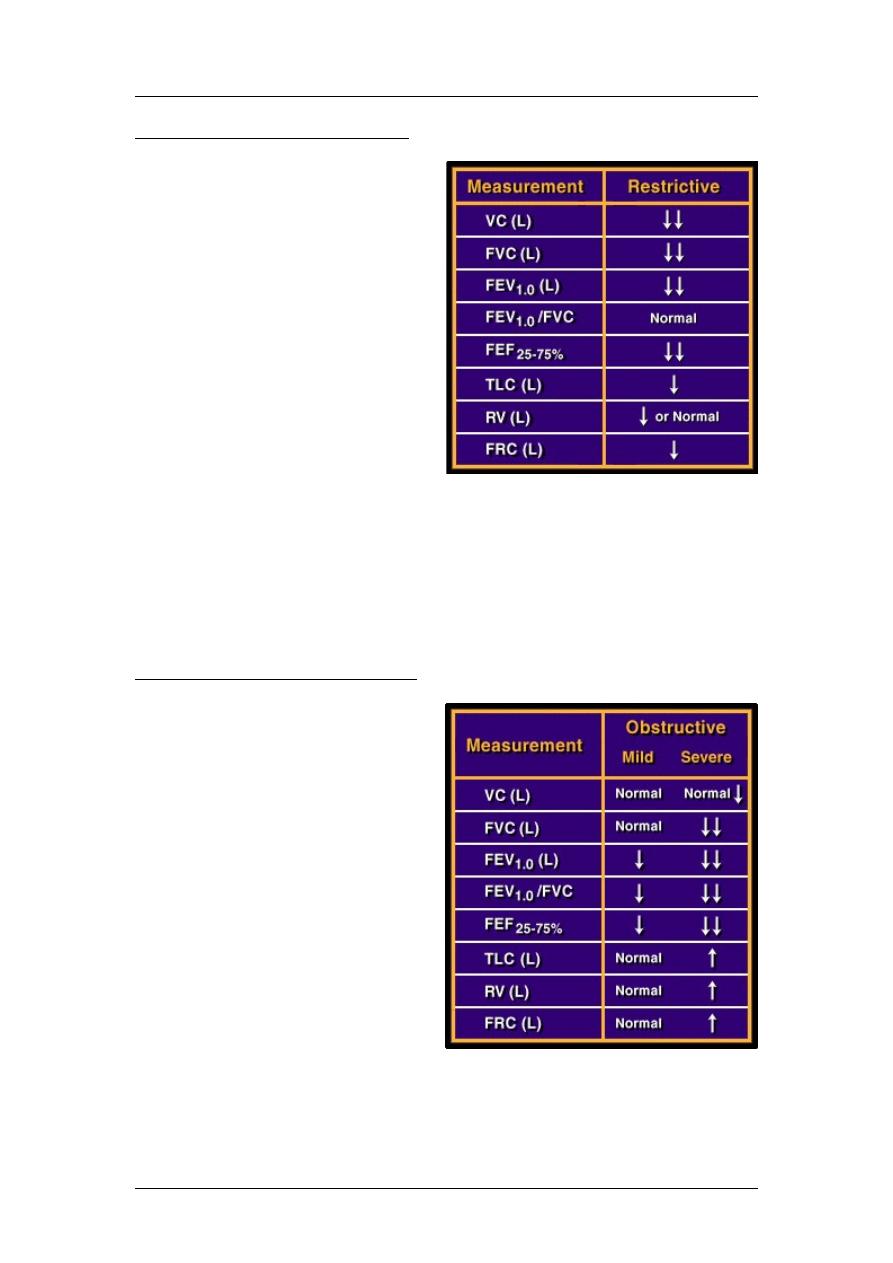
Classification of Lung Disorders by Spirometry
By comparing recorded values of the resting VC, FVC and FEV
1.0
obtained
from the spirogram to the predicted values obtained from nomograms, it is
possible to group respiratory diseases or disorders into two broad cateogories
of restrictive or obstructive impairments.
Respiratory Investigations
1- Blood pH
2- Blood CO2
3- Blood O2
4- Maximum expiratory flow (400ml/min) (Peak Expiratory Flow Meter)
5- FVC (forced vital capacity) and FEV1 (forced vital capacity in the first
second).
26
Respiratory Physiology
Prof. Zaid Al-Madfai
Restrictive Disorders or Diseases
Restrictive impairments are
characterized by limited lung
expansion, reduced lung volumes,
and usually decreased expiratory
flow rates from predicted values.
Thus, the recorded FVC and
FEV
1.0
are below the predicted
normal. However, with a strictly
restrictive disorder, airway
resistance is normal, so the ratio
of the actual FEV
1.0
to the FVC of
the subject is normal (i.e,
FEV
1.0
/FVC> 80%). The loss of
lung volume with restrictive
disorders is reflected by
reductions in other lung volumes
(RV, FRC) and a reduced FEF
25-75%
from predicted values. Some examples of
restrictive disorders include pregnancy, excessive abdominal fat, or even tight-
fitting undergarments that limit normal descent of the diaphragm. Some
restrictive diseases include pulmonary fibrosis, sarcoidosis, pleural effusion,
spinal cord injury that affects innervation to the respiratory muscles, or spinal
nerve paralysis such as with polio. Injury or disease to the respiratory control
centers of the brain stem might also be reflected as a restrictive impairment.
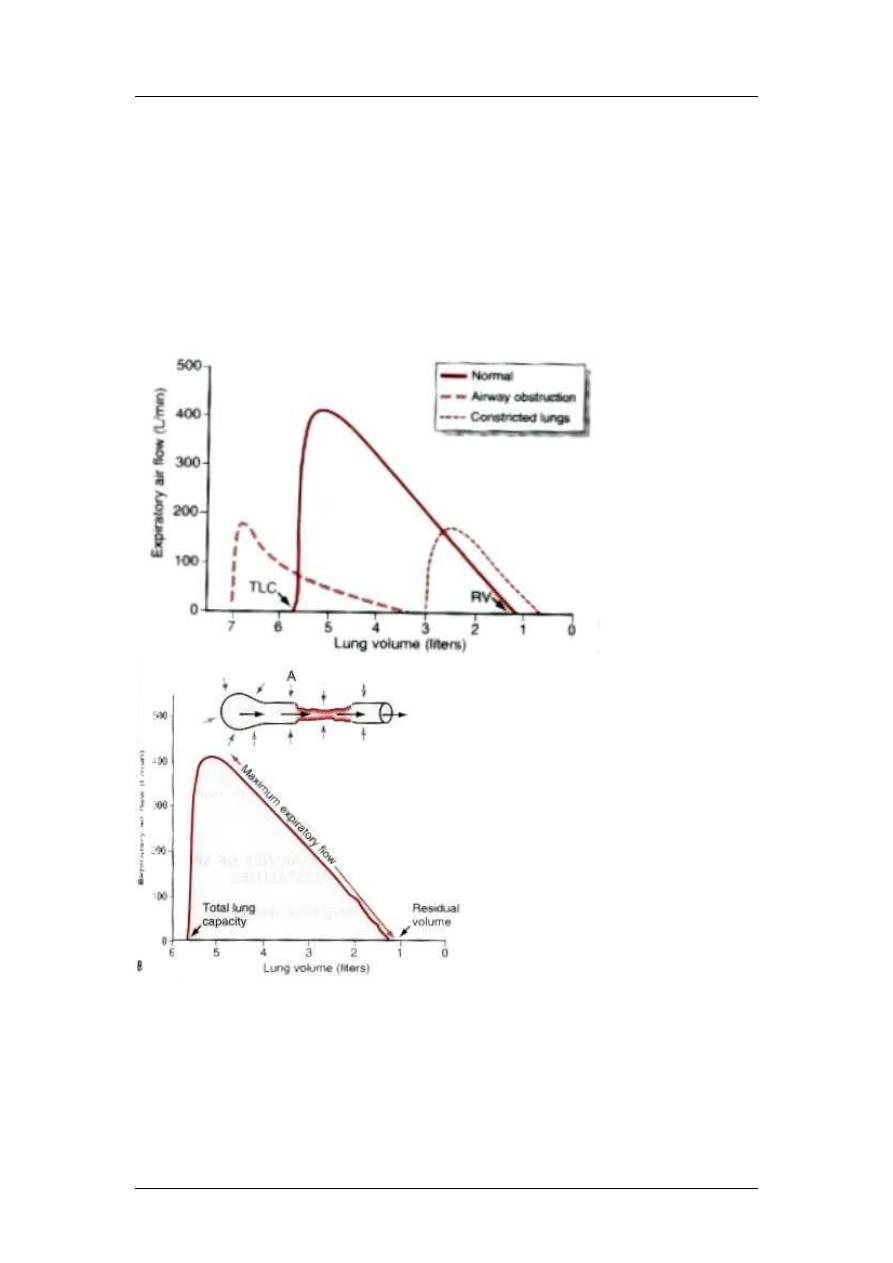
Obstructive Disorders or Diseases
Obstructive impairments are
characterized by increased airway
resistance causing reduced
expiratory airflow rates.
Obstructive disorders are always
associated with airway
dysfunction. Examples of
obstructive diseases include
asthma, chronic bronchitis, and
emphysema. However, even a
severe cold with pulmonary
congestion might be manifested
as an obstructive disorder. With
obstructive impairments, the
actual (recorded) FEV
1.0
/FVC is
less than 80% and the FEV
1.0
and
FEF
25-75%
are 75% or less of the
predicted values. How
obstructive disorders affect other lung volumes, including the FVC, depends
upon the severity or stage of the disease. For example, with mild asthma, the
FVC may be normal but the FEV
1.0
and FEF
25-75%
reduced from normal.
27
Respiratory Physiology
Prof. Zaid Al-Madfai
During the early stages of emphysema, the VC and FVC may be within
normal limits, but with advanced emphysema the FVC is reduced. With
advanced emphysema, the lung becomes hypercompliant (more distensible
with less recoil), leading to air trapping reflected by an increase in the RV and
FRC, even though TLC is unchanged, or possibly increased from normal. If
the FEV
1.0
or FEF
25-75%
increases after inhalation of a bronchodilator (i.e.,
beta-agonist), a portion of the obstruction is likely due to bronchospasm. The
potential reversibilty of an obstructive impairment is indicated when the
FEV
1.0
is increased by 15% or more after inhalation of a bronchodilator.
Abnormalities:
1- Emphysema: excess air in the lungs. Chronic infection increase mucus
chronic obstruction air remain in alveoli overstretching of alveoli
alveolar obstruction. So it leads to obstruction and damage decrease
diffusing capacity very low VA/Q (shunt) and very high VA/Q (dead
space). At the end, damage to alveolar wall damage to capillaries
pulmonary hypertension right sided heart failure.
28

Respiratory Physiology
Prof. Zaid Al-Madfai
2- Pneumonia: any inflammatory condition of the lung where the alveoli are
filled with fluid and blood cells. So in infection, the damage to alveoli
filling with fluid and blood consolidation reduction of available surface
and reduction of VA/Q hypoxemia and hypercapnia.
3- Atelectasis (airway obstruction or lack of surfactant): leads to collapse of the
lungs, so in blockage air entrapment air absorption collapse of alveoli
(pliable lung) or alveoli filled with fluid (rigid lung), so increase resistance to
blood flow and in addition, hypoxia vasodilatation, so blood flow to other
areas and VA/Q is not much suffered.
4- Asthma: spastic contraction of smooth muscles of bronchioles because of
hypersensitivity.
Hypoxia: decrease O2 to the cells. It is divided into (1) circulatory, (2) histotoxic, (3)
anemic, (4) hypoxic hypoxia.
Circulatory Hypoxemia
Circulatory hypoxemia, also known as stagnant hypoxemia, is characterized
by, or a result of inadequate blood flow to a particular tissue. The failure to
deliver adequate O
2
results from a problem with the cardiovascular system.
Circulatory arrest could result from heart failure or vasomotor collapse, or
locally, from vascular disease or emboli that limit blood flow to a particular
organ. If blood flow to the brain is blocked for about 10 seconds,
consciousness is lost, mostly as a result of hypoxemia. In the eye, occlusion of
vessels can lead to vision loss in 6 seconds. With circulatory arrest, products
of anaerobic metabolisms are not cleared. This can potentially compound the
damage from the hypoxemia.
Histotoxic Hypoxemia
With histotoxic hypoxemia, tissues are unable to use O
2
properly because the
enzymes of aerobic metabolism are dysfunctional. Several poisons, such as
cyanide and mercury, interfere with the oxidative enzymes so that O
2
can no
longer serve as the final proton acceptor for the cytochrome enzymes. Arterial
blood PO
2
and content are often normal with histotoxic hypoxemia, whereas
systemic venous and mixed venous blood PO
2
and content are higher than
normal, reflecting the inability of oxidative enzymes to use O
2
.
Anemic Hypoxemia
Anemic hypoxemia is characterized by a low blood O
2
content due to either a
low [Hb] or an inability of Hb to bind and hence transport O
2
. With anemic
hypoxemia, however, the systemic arterial PO
2
is usually close to normal.
Because the arterial chemoreceptors are located in the systemic arterial
circulation and only detect the physically dissolved O
2
(PaO
2
) and not the O
2
attached to Hb (HbO
2
), they can be fooled by this form of hypoxemia. With
anemic hypoxemia, the arterial PO
2
is often close to normal. As a result, the
peripheral chemoreceptors fail to detect any change in blood O
2
content. Also,
29

Respiratory Physiology
Prof. Zaid Al-Madfai
the central chemoreceptors are not responsive to hypoxemia, so breathing is
not markedly stimulated.
Hypoxic Hypoxemia
Hypoxic hypoxemia differs from anemic hypoxemia in that the arterial blood
PO
2
is reduced along with the O
2
content. With hypoxic hypoxemia, breathing
is stimulated by the hypoxemia. The most common clinical example of
hypoxic hypoxemia is a right-to-left shunt, where blood travels through the
lung from the right to left heart without undergoing complete oxygenation.
This is common in conditions where pulmonary diffusion is impaired, so gas
exchange between the alveoli and pulmonary capillary blood is diminished.
Hypoxic hypoxemia can also result from hypoventilation associated with
injury or disease to the brain stem respiratory control centers, spinal cord, or
motor nerves innervating the respiratory muscles. Individuals with
emphysema often exhibit hypoxic hypoxemia characterized by a low arterial
PO
2
and blood O
2
content. However, such individuals may also have an
elevated arterial PCO
2
. Another example of hypoxic hypoxemia is altitude
ascension. This causes a decline in blood PO
2
PO
2
is
reduced with altitude. This decline in the PO
2
causes the peripheral
chemoreceptors to stimulate breathing. The increase ventilation typically
results in a lowering of both blood and CSF PCO
2
and [H
+
]. Diminished levels
of these potent stimuli to breathing can act to counter a portion of the hypoxic
stimulation to ventilation.
Hypercapnia: increase CO2 in body fluids
It is not always associated with hypoxia but only in hypoventilation and circulatory
failure.
Cyanosis: Blue skin due to increase deoxygenated blood. It appears when
deoxygenated blood is more than 5gm/100ml, so it does not appear in anemia.
Dyspnea: mental anguish associated with inability to ventilate enough leading to air
hunger. It is caused by (1) abnormality of respiratory gases in body fluids, specially
hypercapnia, (2) amount of work by respiratory muscles increases, (3) state of the
mind.
30
