
1
Professor Nada Al Alwan
Diagnostic Cytopathology
Definition: Diagnostic or Clinical Cytology is the study of the normal and disease-
altered cells obtained from various sites of the body (i.e., through the detection of
abnormal morphologic characteristics of the examined dissociated human cells).
Cytopathology in Relation to Histopathology
Advantages of Cytopathology (c
ould be summarized in the following Table):
Limitations of Cytopathology:
As a rule, histopathology remains the gold standard technique in diagnostic pathology.
The whole presented tissue definitely provides a more accurate precise diagnosis of
the disease in question. The interpretation of the morphological cellular changes is
based mainly on individual observations and often cannot be forced into rigid criteria.
Histopathology
Cytopathology
Deals with the form and the
structure of the tissue.
Evaluation usually begins with a
tissue biopsy.
More invasive traumatic
procedure is needed; utilizing
surgical instrumentation such as
foreceps, scissors, etc..)
Needles if used should have a
large gauge (i.e., Tru-cut needles
measuring 14, 16 ) .
Diagnosis obtained after days.
Basic stain is H&E
Paraffin blocks are needed
Difficult to identify specific
causative inflammatory pathogen.
Deals with the structural changes
within the nucleus and cytoplasm
of individual cells
Evaluation requires cells only.
Inexpensive simple means of
diagnosis which allows frequent
repetition of cellular sampling
(since it causes no tissue injury).
Fine needles with 22, 23 or 24
gauge are usually preferred.
Rapid diagnosis that could be
obtained within minutes.
Basic stain is Pap stain (however
H&E could be used as well)
Mainly slides are needed
Smears permit better evaluation of
the nature of the inflammatory
process. Fungi and parasites are
usually easier to be diagnosed.

2
Thus, in many cases the cytological diagnosis could not be final and needs
confirmation by histopathology for the following reasons:
Often the nature of the lesion is not so obvious as in a histological section.
The location of the lesion is difficult to be pinpointed by cytology: for example a
squamous cancer cells found in a cytology sputum sample may have originated
from the buccal mucosa, pharynx, larynx or bronchi.
The size of the lesion cannot be approximated by cytology.
The type of the lesion –e.g., in situ carcinoma as compared with early invasion is
more difficult to assess since the relationship of the cells to the surrounding
stroma cannot be determined by cytology.
Sampling Techniques
In general, diagnostic cytology is based upon three basic sampling techniques :
(1) the collection of exfoliated cells,
(2) the collection of cells removed by brushing or similar abrasive techniques,
(3) the aspiration biopsy or removal of cells from nonsurface –bearing tissue (or
deep organs) by means of a needle, with or without a syringe.
1- Exfoliative Cytology
Exfoliative cytology is based on spontaneous shedding of cells derived from the lining
of an organ into a cavity, where they can be removed by nonabrasive means. It is the
simplest of the three sampling techniques. To prevent the deterioration of cells by air-
drying or by enzymatic or bacterial actions, the material should be processed
immediately without delay. Alternatively, the use of fixatives, such as alcohol or other
cell preservatives is indicated.
Typical examples are:
The vaginal smear (Pap smear): The cells that accumulate in the vaginal fornix
are derived from several sources: from the squamous epithelium that lines the
vagina and the vaginal portio of the uterine cervix, from the epithelial lining of
the endocervical canal, and from other more distant sources such as the
endometrium. These cells accumulate in the mucoid material and other secretion
from the uterus and the vagina. In addition to the cells derived from the epithelial
linings, the vaginal fornix often contains leukocytes and macrophages that may

3
accumulate there in response to an inflammatory process, and a variety of
microorganisms such as viruses, bacteria, fungi, and parasites that may inhibit the
lower genital tract.
Sputum examination. The sputum is a collection of mucoid material that
contains cells derived from the buccal cavity, the pharynx, larynx, trachea, the
bronchial tree and the pulmonary alveoli; as well as inflammatory cells,
microorganisms, foreign material , etc… The same principle applies to:
Voided urine
Body fluids
Nipple discharge
2- Abrasive Cytology
The purpose of this procedure is to enrich the sample with cells obtained directly from
the surface of the target of interest. Hence, cell specimens are usually obtained
through superficial scraping of the lesion (artificial mechanical desquamation) .
Examples include:
Cervical scraping through Pap smear:
Buccal mucosal smear
Skin scraping of various lesions
Brushing techniques through using various rigid endoscopic and fibroptic
instruments to collect cell samples from the gastrointestinal tract, bronchial tree,
etc…
The Pap Smear Test (Figures 1 - 3)
Is used mainly to detect precancerous and cancerous lesions of the uterine cervix.
Cervical cancers are caused by Human Papilloma Viruses (HPV). These viruses are
tissue-specific DNA viruses that are easily transmissible and highly prevalent. HPV is
the most common sexually transmitted infection; the vast majority of HPV infections
are transient and could be cleared as a result of natural immune responses, becoming
undetectable after 6 to 18 months. However, precancerous lesions can develop if the
infection persists.
HPV induces cellular changes at the basal layer of the squamous epithelium of the
cervix at the transformation zone (pathologically known as “koilocytotic atypia”).
These changes lead to dysplasia or cervical intraepithelial neoplasia (CIN) and might

4
eventually cause carcinoma. They tend to regress to normal within one year or very
slowly progress to more severe abnormalities and eventually to cervical cancer.
Persistence and progression to cancer may take several years (10-20 years) to develop.
This long natural history makes it liable for early detection and treatment at its
precancerous lesions, if women were screened, diagnosed and treated early.
Thus the Pap smear test is based on the fact that cancer of the cervix is one of the
most preventable cancers, because most of the cellular changes which may lead to
carcinoma can be detected and accordingly treated at an early stage before
progression. .In most cases, cervical carcinoma develops slowly; whereby it passes
into different pre-neoplastic conditions before it reaches the cancer stage.
Mild Dysplasia --► Moderate Dysplasia --► Severe Dysplasia --►
CIN I CIN II CIN III
Carcinoma in Situ --► Carcinoma
CIN III
The CIN classification has almost universally replaced the world health organization
classification, with CIN I, 2 and 3 corresponding to mild, moderate and severe
dysplasia/carcinoma in situ, respectively. The Bethesda Classification system was
introduced in 1988 to facilitate interpretation and management of these precancerous
lesions; whereby LSIL (Low-Grade Squamous Intraepithelial Lesion) stands for CIN I
and Koilocytosis while HSIL (High Grade Squamous Intraepithelial Lesion)
corresponds to CIN II and CIN III.
Microscopical examination of the exfoliated cells from the uterine cervix through the
Pap Smear should therefore lead to the detection of these pre-neoplastic lesions in
their earliest stages (i.e., stage of mild dysplasia ). Accordingly, giving the
appropriate treatment will eventually lead to prevention of cervical cancer.
Hence, Pap Smear test is a simple procedure in which a small number of cells are
collected from the cervix and sent to the laboratory where they are tested for anything
abnormal. The cervical scraper introduced by Ayre in 1947 allows a direct sampling
of cells from the squamous epithelium of the cervix and the adjacent endocervical
canal. No anaesthesia is required, and the diagnosis could be obtained within few
minutes. The procedure could be easily carried out in any clinic or specialized lab.
It is recommended that all women between the ages of 18 and 70 years, who have
ever had sexual activity, are advised to have the test every 2 years.
5
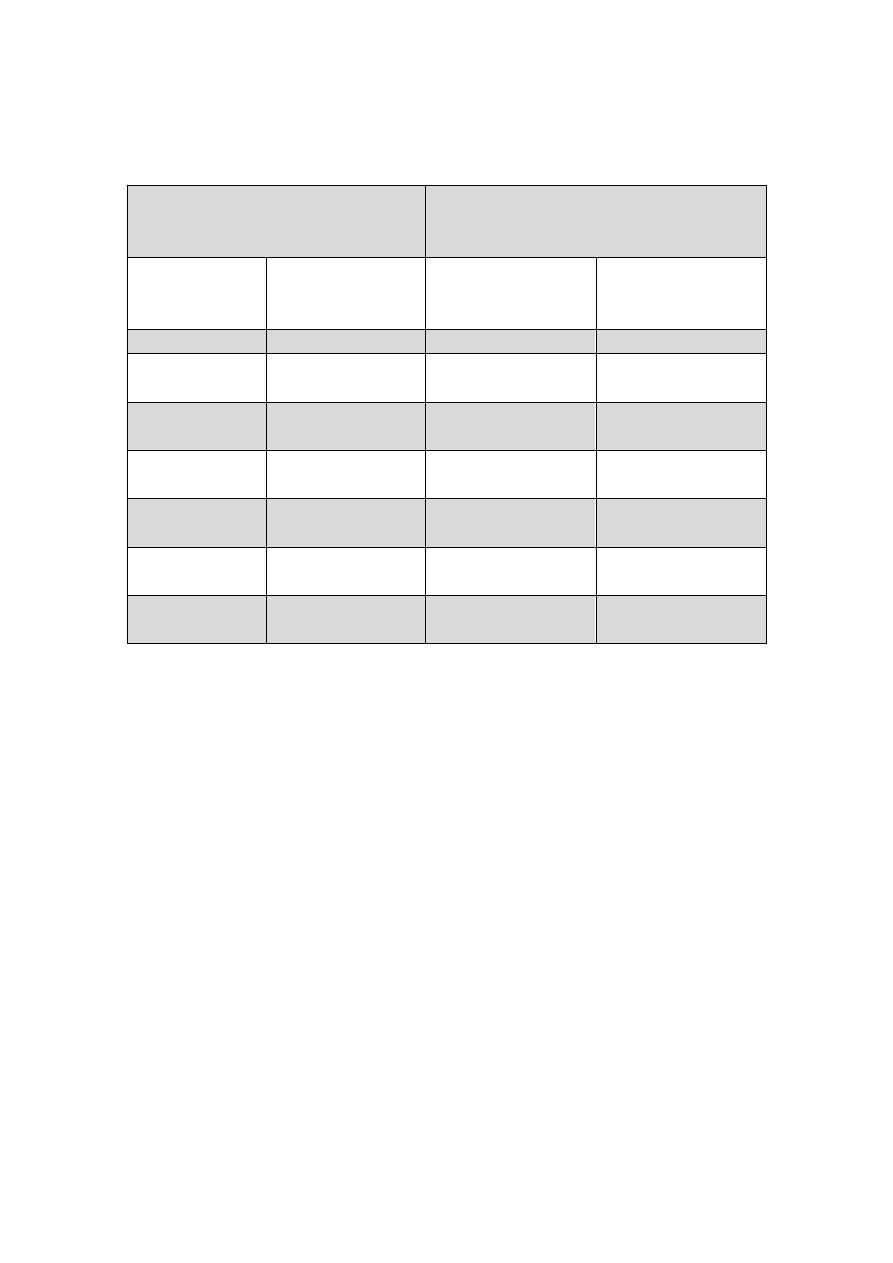
Different Terminologies used for Cytological and Histological Reporting
od Precancerous Lesions of the Uterine Cervix:
The CIN classification has almost universally replaced the World Health Organization
classification, with CIN I, II and III corresponding to mild, moderate and severe
dysplasia/carcinoma in situ, respectively. The Bethesda Classification system was
then introduced in 1988 to facilitate interpretation and management; whereby LSIL
(Low-Grade Squamous Intraepithelial Lesion) stands for CIN I and Koilocytosis
while HSIL (High Grade Squamous Intraepithelial Lesion) corresponds to CIN II and
CIN III.
3- Fine Needle Aspiration Cytology (FNAC) (Figure 4)
In general, the definitive diagnosis of any mass can be established by:
Open biopsy
Tissue core needle (Tru-cut) biopsy
Fine needle aspiration biopsy.
Cytological Classification
Histological Classification
Pap
Bethesda system
CIN
WHO descriptive
classifications
Class I
Normal
Normal
Normal
Class II
ASC-US
ASC-H
Atypia
Atypia
Class III
LSIL
CIN I including flat
condyloma
Koilocytosis
Class III
HSIL
CIN II
Moderate dysplasia
Class III
HSIL
CIN III
Severe dysplasia
Class IV
HSIL
CIN III
Carcinoma in situ
Class V
Invasive carcinoma
Invasive carcinoma
Invasive carcinoma

6
Compared to FNA, Tru-cut biopsy is a more traumatic procedure which should be
performed under local anaesthesia. It requires more time and special equipments
that are more expensive. Pain, discomfort and bleeding are common complications.
FNAC, on the other hand, provides many advantages to the surgeons being an easy,
reliable, cost effective diagnostic technique which could give rapid results. The
procedure could be performed in an office setting without anaesthesia. It is usually
not more painful than a venipuncture and can be repeated immediately if the acquired
material is inadequate.
The National Health Service Breast Screening Program (NHSBSP) displayed that
many centers wished to include FNA as an additional test to provide preoperative
diagnosis of breast cancer and to reduce the number of operations for benign breast
diseases.
When reduced to its simplest terms, FNAC consists of:
Using a needle and syringe to remove material from a mass.
Smearing it on a glass slide.
Applying a routine stain.
Examining it under the microscope.
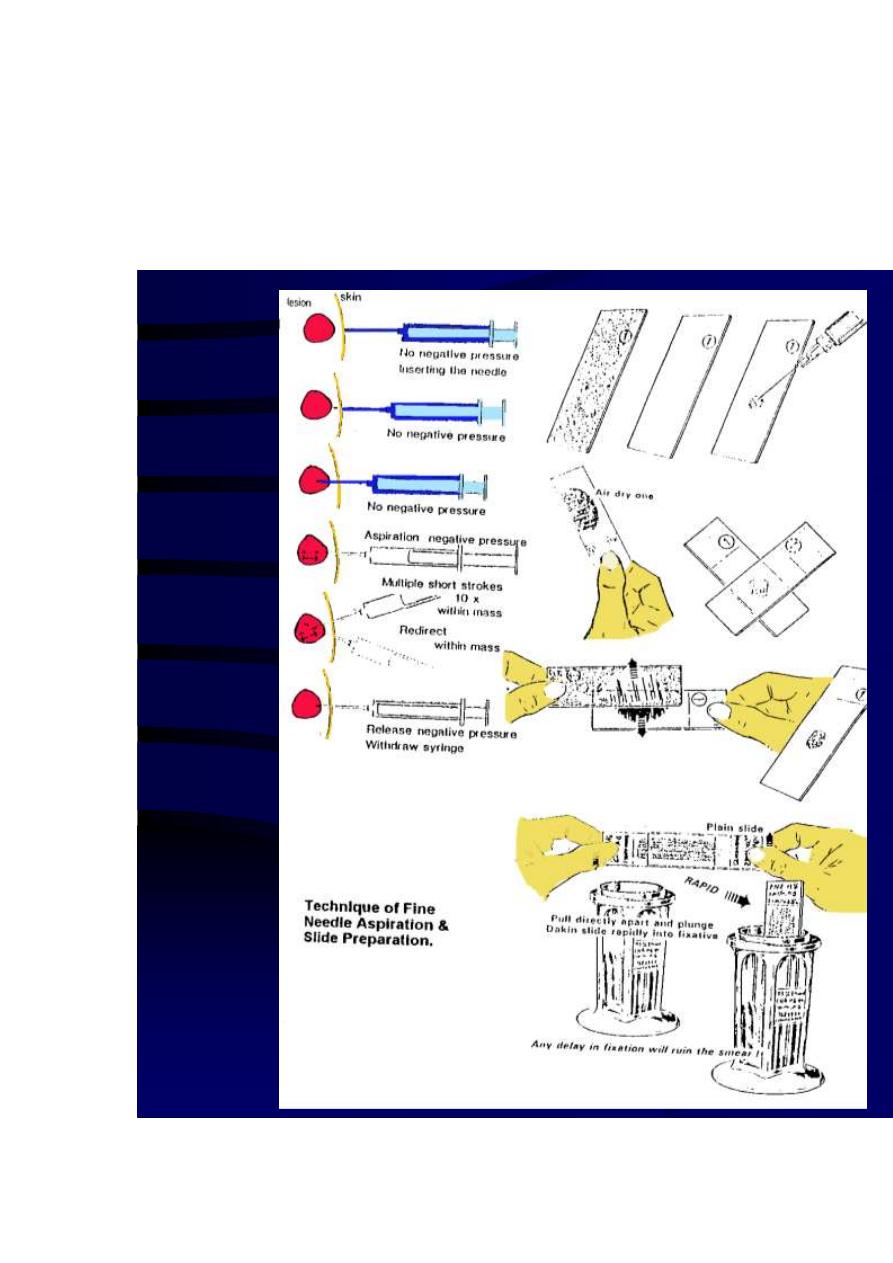
Technique of FNAC:
The skin over the palpable mass (within the breast, lymph node, or any other organ) is
sterilized with an antiseptic. Utilizing the index and the middle finger or the thumb
and the index finger, the mass is localized with the non-dominant hand. With firm
downward pressure on the skin over the mass, it should be compressed against a rib
and stabilized.
Aspirates should be obtained using preferably a 23 gauge, 1 ½ inch disposable needle
mounted on a 10 ml plastic syringe, held by the dominant hand. Larger needles (22
gauges) are used in aspirating material from hard fibrous masses and in cases of
suspected cyst or abscess.
Without using anesthesia, the needle should be gently introduced through the skin
passing to the level of the dominant mass. Having confirmed the position of the
needle within the mass, negative pressure should be created within the syringe by
pulling back the plunger. The needle should move back and forth through the mass, in
different rotational directions using sewing-like-motion. Suction should be maintained
throughout the process by outward pressure of the right thumb on the underside of the
syringe. By this method the needle can cut loose many small pieces of tissue that are
then readily aspirated due to the suction applied by syringe. These to and fro strokes
should be repeated at least 6-8 times. In general most of the aspirations are
terminated when material begins to appear in the needle hub.
7
The following step should be designed to protect the material that has been obtained.
All suction should be released before removing the needle from the mass. This is
accomplished by allowing the syringe plunger to return gently to its resting position.
Then the needle should be withdrawn gently from the mass. To limit haematoma
formation from the site of the puncture, firm pressure should be applied with a piece
of cotton for two minutes.

8
Equipments needed for FNAC procedure:
Syringes
The key feature in a syringe is lightness in weight, adequate in volume, and one hand
control. Modern sterile disposable plastic syringes are perfect for use in FNAC. Most
practitioners use the 10 cc size, while some prefer the 20 cc size (specifically when a
cyst is suspected).
Needles
Several variables should be considered in choosing the proper length and gauge. In
general the length should be at least 1.5 inch (3-8 cm). This is desirable in the breast
because many lesions are found deeper than expected. It has also been demonstrated
that small gauges (22-23) are preferred since they are rigid enough and at the same
time cause less sensation and haematoma. Needles with a plastic hub rather than a
metal hub are preferred as well. This permits the aspirator to monitor the recovery of
tissue, blood or other fluids as they appear in the hub.
Glass Slides
Common routine slides measure 75 mm X 25 mm X 1mm. An important procedure is
slide labeling at the time of sampling. That is why slides which have one frosted end
are preferred. Various substances are used to increase the adherence of specimens to
the slide surface, the most commonly used being albumin.
Fixatives
These are applied to the smears as a spray or by immersion of the slide into a liquid.
The most commonly used is 95 % Ethanol. This inexpensive readily available liquid
provides excellent cytological details. Its only disadvantage is the need to store and
transport slides in a container of liquid and to have them immersed in for at least 20
minutes.
Routine Stains
For cytological diagnosis, fixed material is usually stained by Papanicolaou Stain
(which is preferred) or by Hematoxylin and Eosin (H&E) method. Both employ one
of the Hematoxylins for staining of the nuclei. This dye colors the nucleic acids as a
dark purple blue color. The counter staining with Eosin is designed to show
cytoplasmic characteristics. With the Pap stain one hallmark is the use of Orange-G,
which stains cytoplasmic keratin with a bright orange color.
Air-dried smears on the other hand are usually stained by any Romanowsky stains,
which are various combinations of methylene blue and its breakdown products (Azure
A, B, &C) with Eosin. Most rely on Methanol fixation.
Papanicolaou Stain
All slides should be wet fixed within 95% or absolute Ethanol before staining:
95% ethanol 10 dips
80% ethanol 10 dips
70% ethanol 10 dips
50% ethanol 10 dips
Distilled water 10 dips

9
Hematoxylin Stain 1-2 min.
Running Tap water 10 dips
50% ethanol 10 dips
70% ethanol 10 dips
80% ethanol 10 dips
95% ethanol 10 dips
Orange-G Stain 2 min.
95% ethanol 10 dips
Eosin Stain 2 min.
95% ethanol 10 dips
95% ethanol 10 dips
Absolute ethanol 10 dips
Absolute ethanol: Xylol (50:50 mixture) 5 min.
Xylol 20 min.
Mount with Canada Balsam
Pitfalls to Reliable Results from FNAC
No mass
Vague mass
Mass being too small ( less than 1 cm )
Mass being too deep
Gross blood into the syringe (i.e., RBCs can mask the picture)
Scanty cellularity in the aspirated mass
Dense fibrosis
Gross fluid into th
Indications for Cytopathology
1- Differentiation between benign and malignant lesions.
2- Diagnosis of malignancy and its type, as well as the identification of the
neoplastic cells in primary, metastatic (secondary) or recurrent tumors.
3- Diagnosis of premalignant diseases: i.e., detection of precancerous or
dysplastic cellular changes (figure 5). As explained earlier, dysplasia may be
graded as mild, moderate and severe. In the uterine cervix for example, those
lesions could be eliminated by treatment of the associated inflammation and
causative pathogen or by excision of the lesion.
4- Detection of inflammation and certain types of pathogenic agents: i.e., the
cytologist could prove that the cause of vaginal secretion is vaginitis due to
Trichomonus vaginalis, Moniliasis or the cytology could show changes
suggestive of Human Papilloma Virus infection (HPV – Figure 6). Similarly

11
the cause of cystitis may be related to bilharziasis ( through the detection of
Bilharzial ova in smears of urine samples).
5- Study of the hormonal patterns and evaluation of the gonadal hormonal
activity: through the examination of the squamous cells in vaginal smears;
which are under the influence of ovarian hormones (figure 7).
6- Follow-up and monitoring of response to chemotherapy and irradiation; the
latter producing certain cellular features which could be diagnostic on
cytologic examination.
7- The identification of sex chromosome: if a newborn presents with ambiguous
genitalia, one can not tell whether the sex is male or female. The presence of a
dark dot attached to the nuclear membrane from inside (Barr body +ve)
indicates that a sex chromosome is present, i.e., the genotype of the baby is
XX (♀). Conversely the absence of this Barr body indicates that there is no X
chromosome and accordingly the newborn is genotypically a male ((XY ♂).
8- Tumour markers study on cytological specimens.
Cytological Criteria of Malignancy
(Figures 8 – 12)
A) Nuclear Changes:
Nuclear hypertrophy: nuclear enlargement that leads to increased N/C ratio.
Nuclear size variation
Nuclear shape variation
Hyperchromatism and chromatin irregularity: refers to increased chromatin
materials. In malignant cells the chromatin is not evenly distributed within the
nucleus; it is also distributed as coarse, clumps. This in contradistinction to
normal cells, which have evenly distributed chromatin.
Multinucleation: malignant cells may contain more than one nucleus. However,
some normal cells such as hepatocytes and histiocytes may contain more than
one nucleus. Multinucleated malignant cells differ from nonmalignant
multinucleated cells by the fact that the nuclei of malignant cells are unequal
in size (in contrast to that of normal cells).
Irregularity of the nuclear membrane.

11
Irregular and prominent nucleoli: giant nucleoli or multiple nucleoli may be
present that differ in their sizes and shapes. It should be remembered, however,
that normal columnar and goblet cells may contain 2 nucleoli.
B) Cytoplasmic Changes:
Scantiness of cytoplasm: in consequence to the high N/C ratio.
Cytoplasmic boundries: sharp and distinct in Squamous cell carcinomas and
indistinct in undifferentiated carcinomas.
Variation in size .
Variation in Shape.
Cytoplasmic staining: deep orange in keratinizing squamous carcinomas
or basophoilic in immature poorly differentiated carcinomas.
Cytoplasmic inclusions: e.g. melanin pigments in melanoma.
Cytoplasmic and nuclear membrane relationship: cytoplasmic borders of
malignant cells could be tightly molded against the nucleus, touching it in
more than one place.
C) Changes in Malignant Cells as a Group:
Cellular phagocytosis or Cannibalism: i.e., one cell appearing to be contained
in a vacuole of the cytoplasm of another epithelial cell; indicating rapid
growth of cells within a narrow cavity.
Variation in the size and shape of the cell clusters or sheets.
Lack of cellular adhesion: due to abnormalities in the desmosomes.
Abnormal mitosis: malignant nuclei may show multiple poles e.g. three poles
(tripolar mitosis; triploidy) or four poles (tetrapolar mitosis; tetraploidy). This
is abnormal since normal mitosis has two poles (bipolar). Thus normal cells
show euploid or diploid pattern on flow or image cytometry whereas
malignant cells may show abnormal aneuploid patterns.
Bloody background: fresh blood is meaningless, but malignancy is suspected
when the blood is old, partially ingested by histeocytes or present within a
specimen which is obtained without trauma.
Foreign cellular structures: e.g. psammoma bodies in a routine vaginal smear.
Degeneration and inflammation as a result of erosion or necrosis within the
malignant tumour which could indicate invasion (i.e., tumour diathesis).

12
Perhaps the best demonstrable tool to observe the various types of malignant cells
which could be encountered cytologically is through studying the different variants of
Bronchogenic Carcinoma. A routine recommendation for these patients is the
examination of three successive early morning sputum samples.
Histologically, there are four major different types of bronchial cell carcinoma could
be recognized on cytological examination:
1. Squamous Cell Carcinoma (Figure 9)
Is the most common and easiest type to be diagnosed by cytologic examination of
sputum because of its central position within the bronchial tree. Cytologically, most
malignant cells exfoliate singly but some may be observed in clusters or sheets. Cells
often assume variable sizes and shapes; could be amoeboid in shape, assuming
pseudopod-like projections. Spindle or tadpole cells could be also detected. The
background is usually obscured by necrotic debries, mucous and RBCs (tumour
diathesis).
The cytoplasm is abundant, dense and granular with a glassy orange appearance in
well-differentiated types due to the presence of keratin (stained by Orane G).
Anucleated deep orange squames may be evident in long standing cases. The nucleus
may show nuclear size and shape variation with irregularity of the nuclear membrane.
Marked hyperchromasia is often present; the nuclei appearing very dark or pyknotic.
Cannibalism is common. Red prominent nucleoli could be present.
2. Adeno Carcinoma (Figure 10)
Usually periphral in position. Cells exfoliate in clusters, sheets or acini; rarely singly.
They are often round, oval and irregular in shape. Cytoplasmic vacuoles are observed
in well-differentiated types due to the presence of mucous droplets. Large vacuoles
may push or compress the nucleus to one side giving an irregular moon-shaped
appearance: signet-ring pattern. Neutrophils maybe seen within these vacuoles.
Nuclei are often round or oval with moderate hyperchromatism and irregular nuclear
membrane. Single or multiple diagnostic nucleoli are usually found. Multinucleatin
may occur. Cells stain positive with PAS stain (due to the presence of mucin).
3. Undifferentiated Small Cell Carcinoma (Figure 11)
The WHO classification recognizes three histological subtypes:
- Oat cell carcinoma.

13
- Small cell carcinoma – intermediate type.
- Combined Oat cell carcinoma (seen with foci of squamous cell
and/or adenocarcinoma).
The cellular morphology of small cell carcinoma varies with the method of specimen
collection. In sputum, the exfoliated cells are often small in association with long
strands of mucous. Dark lines of elongated compact masses of numerous small
hyperchromatic neoplastic cells are seen with satellite single cells scattered around.
The nucleus could be degenerated and pyknotic. In brushings and FNA samples, cells
are usually better preserved, appearing larger and displaying more variations in
nuclear chromasia and chromatin patterns.
4. Undifferentiated Large Cell Carcinoma (Figure 12)
These are epithelial tumours comprised of malignant cells with large nuclei and
prominent nucleoli that show no evidence of squamous, glandular or small cell
differentiation. In the WHO classification, two variants are recognized:
- Giant cell carcinoma which contains a prominant component of highly
pleomorphic multinucleated cells which maybe actively phagocytic. The
hyperchromatic nuclei shows irregular chromatin clumping and large
prominent macronucleoli.
- Clear cell carcinoma which is a rare variant composed of large cells with
clear or foamy cytoplasm without mucin.
In general, during the evaluation of a smear, the cytopathologist should look for the
following changes
Modification of the normal nuclear and cytoplasmic cells.
Maturation status (i.e., observe whether the cells are mature or immature.)
The quantity of the cells (hypo- or hyper-cellular) and their mode of
desquamation (clusters, sheets or scattered individually).
Smear background (i.e., the presence of leukocytes, histiocytes, RBCs,
necrotic cells and protein deposits)..

14
