
Normal menstrual cycle
Introduction
The external manifestation of a normal menstrual
cycle is the presence of regular
vaginal bleeding. This
occurs as a result of the shedding of the endometrial lining
following failure of fertilization of the oocyte or failure of implantation. The cycle
depends on changes occurring within the ovaries and fluctuation in ovarian hormone
levels, that are themselves controlled by the pituitary and hypothalamus, the
hypothalamo
–pituitary–ovarian axis (HPO)
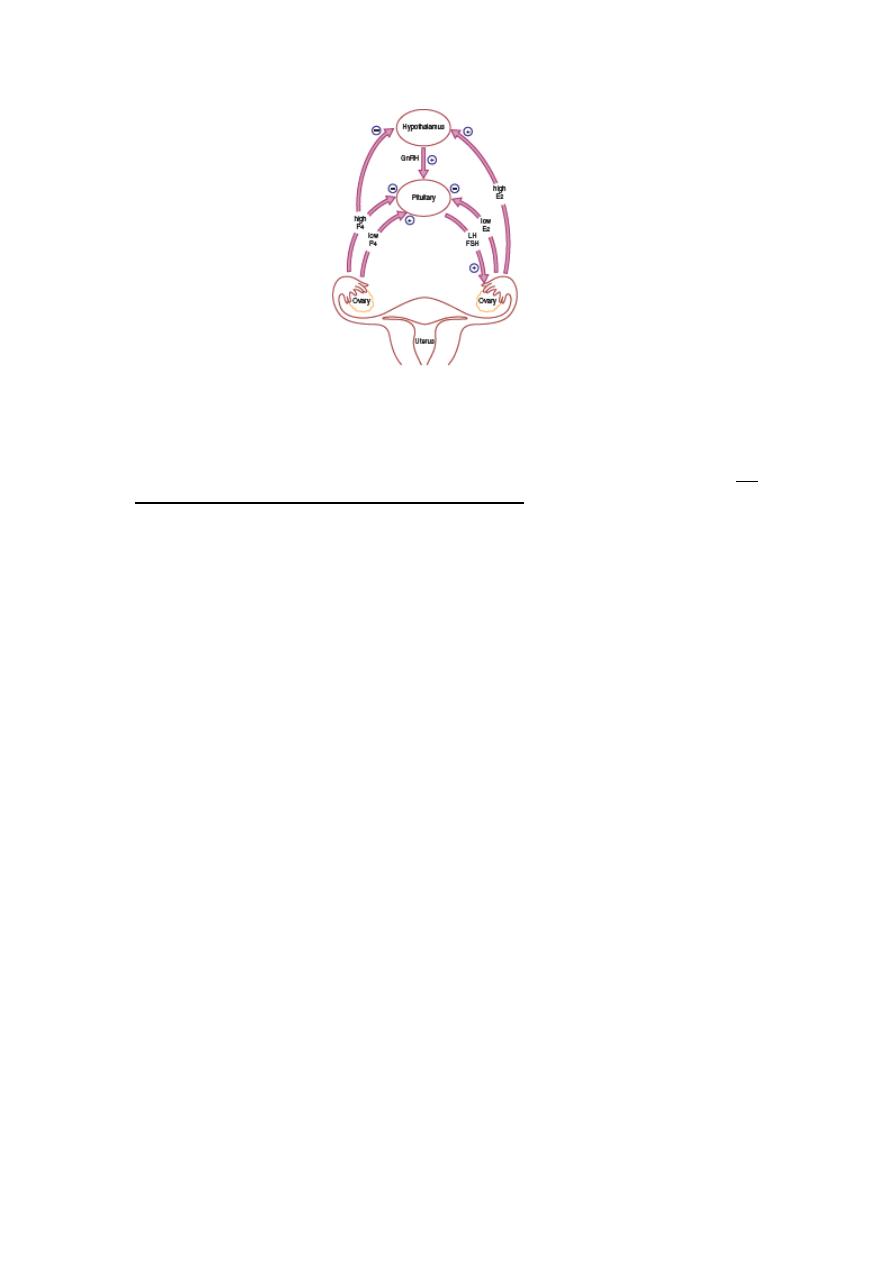
Hypothalamus
The hypothalamus in the forebrain secretes the peptide hormone gonadotrophin-
releasing hormone (GnRH), which in turn controls pituitary hormone secretion.
GnRH must be released in a pulsatile fashion to stimulate pituitary secretion of
luteinizing hormone (LH) and follicle stimulating hormone (FSH). If GnRH is given
in a constant high dose, it desensitizes the GnRH receptor and reduces LH and FSH
release.
Pituitary gland
GnRH stimulation of the basophil cells in the anterior pituitary gland causes synthesis
and release of the gonadotrophic hormones, FSH and LH. This process is modulated
by the ovarian sex steroid hormones oestrogen and progesterone. Low levels of
oestrogen have an inhibitory effect on LH production (negative feedback), whereas
high levels of oestrogen will increase LH production (positive feedback). The high
levels of circulating oestrogen in the late follicular phase of the ovary act via the
positive feedback mechanism to generate a periovulatory LH surge from the pituitary.
Unlike oestrogen, low levels of progesterone have a positive feedback effect on
pituitary LH and FSH secretion (as seen immediately prior to ovulation) and
contribute to the FSH surge. High levels of progesterone, as seen in the luteal phase,
inhibit pituitary LH and FSH production. Positive feedback effects of progesterone
occur via increasing sensitivity to GnRH in the pituitary. Negative feedback effects
are generated through both decreased GnRH production from the hypothalamus and
decreased sensitivity to GnRH in the pituitary. It is known that progesterone can only
have these effects on gonadotropic hormone release after priming by oestrogen.
Inhibin and activin are peptide hormones produced by granulosa cells in the ovaries,
with opposing effects on gonadotrophin production. Inhibin inhibits pituitary FSH
secretion, whereas activin stimulates it.
Ovary
Ovaries with developing oocytes are present in the female fetus from an early stage of
development. By the end of the second trimester
in utero, the number of oocytes has
reached a maximum and they arrest at the first prophase step in meiotic division. No
new oocytes are formed during the female lifetime.
With the onset of menarche, the primordial follicles containing oocytes will activate
and grow in a cyclical fashion, causing ovulation and subsequent menstruation in the
event of non-fertilization. In the course of a normal menstrual cycle, the ovary will go
through three phases:
1
Follicular phase
2
Ovulation
3
Luteal phase.
Follicular phase
The initial stages of follicular development are independent of hormone stimulation.
FSH levels rise in the first days of the menstrual cycle, when oestrogen, progesterone
and inhibin levels are low. This stimulates a cohort of small antral follicles on the
ovaries to grow.
Within the follicles, there are two cell types which are involved in the processing of
steroids, including oestrogen and progesterone. These are the theca and the
granulosa cells, which respond to LH and FSH stimulation, respectively. LH
stimulates production of androgens from cholesterol within theca cells. These
androgens are converted into oestrogens by the process of aromatization in granulosa
cells, under the influence of FSH.
Both FSH and LH are required to generate a normal cycle with adequate amounts of
oestrogen.
As the follicles grow and oestrogen secretion increases, there is negative feedback on
the pituitary
to decrease FSH secretion. This assists in the selection of one follicle to
continue in its development towards ovulation
– the dominant follicle. In the ovary,
the follicle which has the most efficient aromatase
activity and highest concentration
of FSH-induced LH receptors will be the most likely to survive as FSH levels drop,
while smaller follicles will undergo atresia.
The dominant follicle will go on producing oestrogen and also inhibin, which
enhances androgen synthesis under LH control.

There are other autocrine and paracrine mediators playing a role in the follicular
phase of the menstrual cycle. These include inhibin and activin.
Insulin-like growth factors (IGF-I, IGF-II) act as paracrine regulators. Circulating
levels do not change during the menstrual cycle, but follicular fluid levels increase
towards ovulation, with the highest level found in the dominant follicle.
In the follicular phase, IGF-I is produced by theca cells under the action of LH.
Within the theca, IGF-I augments LH-induced steroidogenesis.
In granulosa cells, IGF-I augments the stimulatory effects of FSH on mitosis,
aromatase activity and inhibin production. In the preovulatory follicle,
IGF-I enhances LH-induced progesterone production from granulosa cells. Following
ovulation, IGF-II is produced from luteinized granulosa cells, and acts in an autocrine
manner to augment LH-induced proliferation of granulosa cells.
Kisspeptins are proteins which have more recently been found to play a role in
regulation of the HPO axis, via the mediation of the metabolic hormone leptin
’s effect
on the hypothalamus. Leptin is thought to be key in the relationship between energy
production, weight and reproductive health. Mutations in the kisspeptin receptor, are
associated with delayed or absent puberty,
Ovulation
By the end of the follicular phase, which lasts an average of 14 days, the dominant
follicle has grown to approximately 20 mm in diameter. As the follicle matures, FSH
induces LH receptors on the granulose cells and prepare for the signal for ovulation.
Production of oestrogen increases until they reach the necessary threshold to exert a
positive feedback effort on the hypothalamus and pituitary to cause the LH surge.
This occurs over 24
–36 hours, during which time the LH-induced luteinization of
granulosa cells in the dominant follicle causes progesterone to be produced, adding
further to the positive feedback for LH secretion and causing a small periovulatory
rise in FSH. Androgens, synthesized in the theca cells, also rise around the time of
ovulation .
The LH surge is one of the best predictors of imminent ovulation,
The LH surge has another function in stimulating the resumption of meiosis in the
oocyte just prior to its release.
The physical ovulation of the oocyte occurs after breakdown of the follicular wall
occurs under the influence of LH, FSH and progesterone controlled
proteolytic enzymes, such as plasminogen activators and prostaglandins. There
appears to be an inflammatory-type response within the follicle wall which may assist
in extrusion of the oocyte by stimulating smooth muscle activity. So inhibition of
prostaglandin production may result in failure of ovulation. Thus, women wishing to
become pregnant should be advised to avoid taking prostaglandin synthetase
inhibitors, such as aspirin and ibuprofen, which may inhibit oocyte release.
Luteal phase
After the release of the oocyte, the remaining granulose and theca cells on the ovary
form the corpus luteum.
The granulosa cells have a vacuolated appearance with accumulated yellow pigment,
hence the name corpus luteum (
‘yellow body’). The corpus luteum undergoes

extensive vascularization in order to supply granulosa cells with a rich blood supply
for continued steroidogenesis.
Ongoing pituitary LH secretion and granulosa cell activity ensures a supply of
progesterone which stabilizes the endometrium in preparation for pregnancy.
Progesterone levels are at their highest in the cycle during the luteal phase. This also
has the effect of suppressing FSH and LH secretion to a level that will not produce
further follicular growth in the ovary during that cycle.
The luteal phase lasts 14 days in most women, without great variation. In the absence
of beta human chorionic gonadotrophin (
HCG) being produced from an implanting
embryo, the corpus luteum will regress in a process known as luteolysis. The mature
corpus luteum is less sensitive to LH, produces less progesterone, and will gradually
disappear from the ovary. The withdrawal of progesterone has the effect on the uterus
of causing shedding of the endometrium and thus menstruation. Reduction in levels of
progesterone, oestrogen and inhibin feeding back to the pituitary cause increased
secretion of gonadotrophic hormones, particularly FSH. New preantral follicles begin
to be stimulated and the cycle begins anew.
Endometrium
The hormone changes effected by the HPO axis during the menstrual cycle will occur
whether the uterus is present or not. However, the specific secondary
changes in the
uterine endometrium give the most
obvious external sign of regular cycles.
Menstruation
The endometrium is under the influence of sex steroids that circulate in females of
reproductive age. Sequential exposure to oestrogen and progesterone will result in
cellular proliferation and differentiation, in preparation for the implantation of an
embryo in the event of pregnancy, followed by regular bleeding in response to
progesterone withdrawal if the corpus luteum regresses. During the ovarian follicular
phase, the endometrium undergoes proliferation (the
‘proliferative phase’); during
the ovarian luteal phase, it has its
‘secretory phase’. Decidualization, the formation
of a specialized glandular endometrium, is an irreversible process and apoptosis
occurs if there is no embryo implantation. Menstruation (day 1) is the shedding of
the
‘dead’ endometrium and ceases as the endometrium regenerates (which normally
happens by day 5
–6 of the cycle).
The endometrium is composed of two layers, the uppermost of which is shed during
menstruation. A fall in circulating levels of oestrogen and progesterone approximately
14 days after ovulation leads to loss of tissue fluid, vasoconstriction of spiral
arterioles and distal ischaemia. This results in tissue breakdown, and loss of the upper
layer along with bleeding from fragments of the remaining arterioles is seen as
menstrual bleeding. Enhanced fibrinolysis reduces clotting.
Vaginal bleeding will cease after 5
–10 days as arterioles vasoconstrict and the
endometrium begins to regenerate. Haemostasis in the uterine endometrium is
different from haemostasis elsewhere in the body as it does not involve the processes
of clot formation and fibrosis.
Prostaglandin F2
, endothelin-1 and plateletmactivating factor (PAF) are
vasoconstrictors which are produced within the endometrium and are thought likely to
be involved in vessel constriction, both initiating and controlling menstruation. They
may be balanced by the effect of vasodilator agents, such as prostaglandin E2,

prostacyclin (PGI) and nitric oxide (NO), which are also produced by the
endometrium. Progesterone withdrawal increases endometrial prostaglandin (PG)
synthesis and decreases PG metabolism. The COX-2 enzyme and chemokines are
involved in PG synthesis and this is likely to be the target of non-steroidal anti-
inflammatory agents used for the treatment of heavy and painful periods.
Endometrial repair involves both glandular and stromal regeneration and
angiogenesis to reconstitute the endometrial vasculature. VEGF and fibroblast growth
factor (FGF) are found within the endometrium and both are powerful angiogenic
agents. Other growth factors, such as transforming growth factors (TGFs), epidermal
growth factor (EGF) and IGFs, and the interleukins may also be important.
The proliferative phase
Menstruation will normally cease after 5
–7 days, once endometrial repair is complete.
After this time, the endometrium enters the proliferative phase, when glandular and
stromal growth occur. The epithelium lining the endometrial glands changes from a
single layer of columnar cells to a pseudostratified epithelium with frequent mitoses.
The stroma is infiltrated by cells derived from the bone marrow . Endometrial
thickness increases rapidly, from 0.5 mm at menstruation to 3.5
–5 mm at the end of
the proliferative phase.
The secretory phase
After ovulation (generally around day 14), there is a period of endometrial glandular
secretory activity. Following the progesterone surge, the oestrogen induced cellular
proliferation is inhibited and the endometrial thickness does not increase any further.
However, the endometrial glands will become more tortuous, spiral arteries will grow,
and fluid is secreted into glandular cells and into the uterine lumen. Later in the
secretory phase, progesterone induces the formation of a temporary layer, known as
the decidua, in the endometrial stroma. Histologically, this is seen as occurring
around blood vessels. Stromal cells show increased mitotic activity, nuclear
enlargement and generation of a basement membrane
Recent research into infertility has identified apical membrane projections of the
endometrial epithelial cells known as pinopodes, which appear after day 21
–22 and
appear to be a progesterone-dependent stage in making the endometrium receptive for
embryo implantation .
Immediately prior to menstruation, three distinct layers of endometrium can be
seen. The basalis is the lower 25 per cent of the endometrium, which will
remain
throughout menstruation and shows few
changes during the menstrual cycle. The mid-
portion is the stratum spongiosum with oedematous stroma and exhausted glands.
The superficial portion (upper 25 per cent) is the stratum compactum with
prominent decidualized stromal cells. On the withdrawal of both oestrogen and
progesterone, the decidua will collapse, with vasoconstriction and relaxation of spiral
arteries and shedding of the outer layers of the endometriu
m

