
Dr. HANAN AL – TAEE
DEPARTMENT OF PHYSIOLOGY
Endocrine Functions of Pancreas
O B J E C T I V E S
After reading this lecture, you should be able to:
List the hormones that affect the plasma glucose concentration and briefly describe the
action of each.
Describe the structure of the pancreatic islets and name the hormones secreted by each of
the cell types in the islets.
Describe the structure of glucagon and list the physiologically significant effects of glucagon
and the factors that regulate glucagon secretion.
Describe the structure of insulin and outline the steps involved in its biosynthesis and release
into the bloodstream.
List the consequences of insulin deficiency and explain how each of these abnormalities is
produced.
Describe insulin receptors, the way they mediate the effects of insulin, and the way they are
regulated.
List the major factors that affect the secretion of insulin.
Understand the major differences between type 1 and type 2 diabetes.
REGULATION OF BLOOD GLUCOS LEVEL:
NORMAL BLOOD GLUCOSE LEVE: In normal persons, blood glucose level is controlled within a
narrow range. In the early morning after overnight fasting, the blood glucose level is low
ranging between 70 and 110 mg/dL of blood. Between first and second hour after meals
(postprandial), the blood glucose level rises to 100 to 140 mg/dL. Glucose level in blood is
brought back to normal at the end of second hour after the meals. Blood glucose regulating
mechanism is operated through liver and muscle by the influence of the pancreatic hormones –

insulin and glucagon. Many other hormones are also involved in the regulation of blood glucose
level. Among all the hormones, insulin is the only hormone that reduces the blood glucose level
and it is called the antidiabetogenic hormone. The hormones which increase blood glucose
level are called diabetogenic hormones or anti‐insulin hormones.
Necessity of Regulation of Blood Glucose Level:
Regulation of blood glucose (sugar) level is very essential because, glucose is the only nutrient
that is utilized for energy by many tissues such as brain tissues, retina and germinal epithelium
of the gonads.
ROLE OF LIVER IN THE MAINTENANCE OF BLOOD GLUCOSE LEVEL
Liver
serves as an important
glucose buffer system
. When blood glucose level
increases after a meal, the excess glucose is converted into glycogen and stored in liver.
Afterwards, when blood glucose level falls, the glycogen in liver is converted into glucose and
released into the blood. The storage of glycogen and release of glucose from liver are mainly
regulated by insulin and glucagon.
Insulin helps to control the blood glucose level, especially after meals, when it increases.
Glucagon and other hormones help to maintain the blood glucose level by raising it in between
the meals.
The brain cells are permeable to glucose and can use glucose without the intermediation of
insulin.The brain cells are also quite different from most other cells of the body in that they
normally use only glucose for energy and can use other energy substrates, such as fats, only
with difficulty. Therefore, it is essential that the blood glucose level always be maintained
above a critical level, which is one of the most important functions of the blood glucose
control system. When the blood glucose falls too low, into the range of 20 to 50 mg/100 ml,
symptoms of hypoglycemic shock develop, characterized by progressive nervous irritability
that leads to fainting, seizures, and even coma.
Other hormones which increase the blood glucose level are: Growth hormone, Thyroxin ,
Cortisol , Adrenaline .
Physiologic Anatomy of the Pancreas. The pancreas is composed of two major types of tissues,
as shown in Figure: (1) the acini, which secrete digestive juices into the duodenum, and (2) the
islets of Langerhans, which secrete insulin and glucagon directly into the blood. The human
pancreas has 1 to 2 million islets of Langerhans (constitute 2% of pancreatic tissues mainly in
the tail of pancreas, each only about 0.3 millimeter in diameter and organized around small
capillaries into which its cells secrete their hormones.
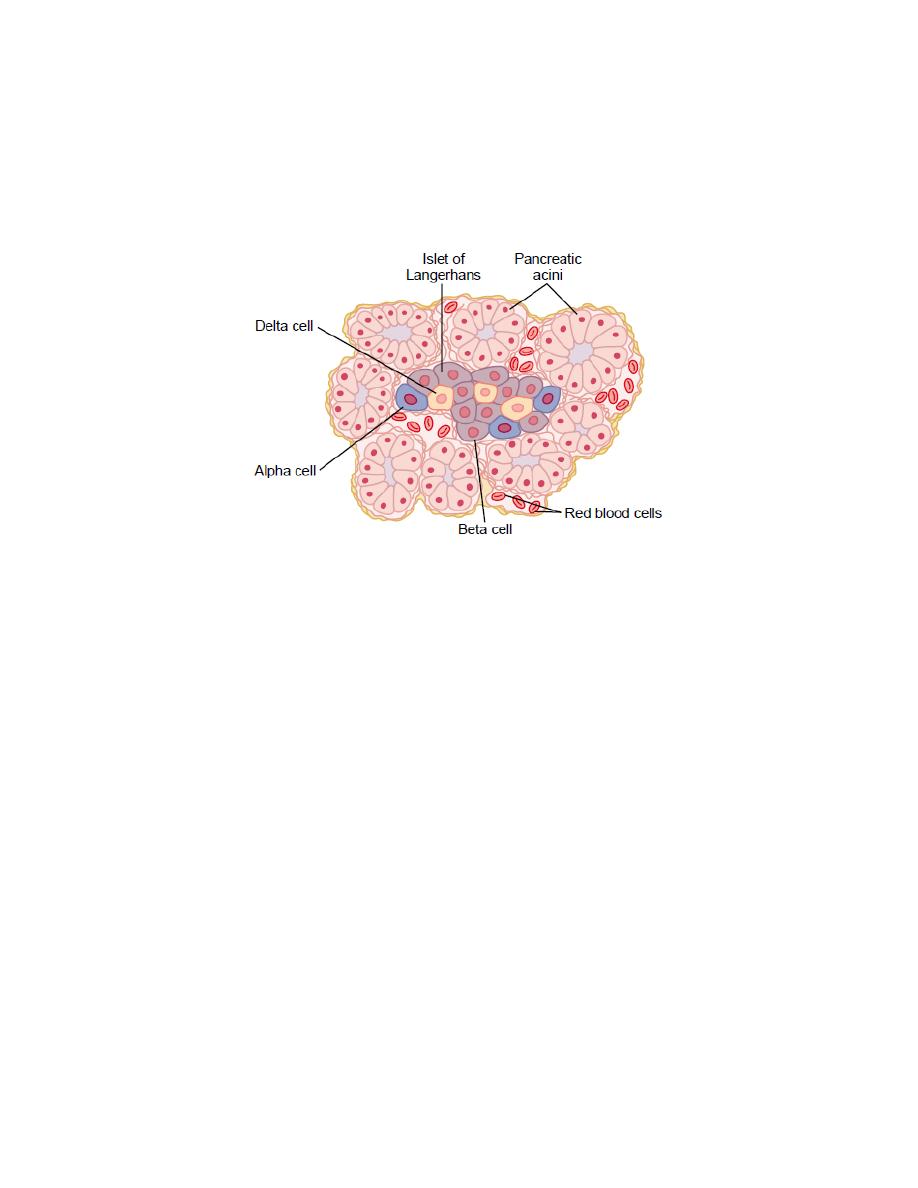
Islets of Langerhans consist of four types of cells: which are distinguished from one another by
their morphological and staining characteristics.
Figure 1: Demonstrate islet of langerhans
1. A cells or α‐cells, which secrete glucagon (constitute about 25 per cent of the total), secrete
glucagon.
2. B cells or β‐cells, which secrete insulin and amylin, a hormone that is often secreted in
parallel with insulin, although its function is unclear. (60 per cent of all the cells).
3. D cells or δ‐cells, which secrete somatostatins, about 10 percent of the total, secrete
somatostatin, plays a role in the regulation of islet cell secretion.
4. F cells or PP cells, which secrete pancreatic polypeptide, a hormone of uncertain function it is
probably concerned primarily with the regulation of HCO–3 secretion to the intestine
The close interrelations among these cell types in the islets of Langerhans allow cell‐to‐cell
communication and direct control of secretion of some of the hormones by the other
hormones. For instance, insulin inhibits glucagon secretion, amylin inhibits insulin secretion,
and somatostatin inhibits the secretion of both insulin and glucagon.

GLUCAGON
Is secreted from A cells or α‐cells in the islets of Langerhans of pancreas. It is also
secreted from A cells of stomach and L cells of intestine.
Is a polypeptide with a molecular weight of 3,485. It contains 29 amino acids. Half‐life of
glucagon is 3 to 6 minutes.
Is synthesized from the preprohormone precursor called preproglucagon in the α‐cells
of islets. Preproglucagon is converted into proglucagon, which gives rise to glucagon.
About 30% of glucagon is degraded in liver and 20% in kidney. The cleaved glucagon
fragments are excreted through urine. 50% of the circulating glucagon is degraded in
blood itself by enzymes such as serine and cysteine proteases.
Actions are antagonistic to those of insulin. It increases the blood glucose level, by
enhancing glycogenolysis, gluconeogenesis, Glucagon shows lipolytic and ketogenic
actions.
Regulation of glucagon secretion
Secretion of glucagon is controlled mainly by glucose and amino acid levels in the blood.
Factors which increase glucagon secretion:
i. Exercise. ii. Stress. iii. Gastrin. iv. Cholecystokinin (CCK). v. Cortisol.
Factors which inhibit glucagon secretion:
i. Somatostatin. ii. Insulin. iii. Free fatty acids. iv. Ketones.
INSULIN:
Is secreted by B cells or the β‐cells in the islets of Langerhans of pancreas.
First isolated from the pancreas in 1922 by Banting and Best.
Is a polypeptide with 51 amino acids and a molecular weight of 5,808.
It has two amino acid chains called α and β chains, which are linked by disulfide bridges.
The α‐chain of insulin contains 21 amino acids and β‐chain contains 30 amino acids.
The biological Half‐life is 5 minutes. Basal level of insulin in plasma is 10 μU/mL.
Synthesis occurs in the rough endoplasmic reticulum of β‐cells in islets of Langerhans. It
is synthesized as preproinsulin, which gives rise to proinsulin. Proinsulin is converted
into insulin and C peptide through a series of peptic cleavages.( C peptide is a
connecting peptide that connects α and β chains, at the time of secretion the C peptide
is detached).
Preproinsulin → Proinsulin Peptic cleavage Insulin

METABOLISM
When insulin is secreted into the blood, it circulates almost entirely in an unbound
form; it has
a plasma half‐life that averages only about 6 minutes, so that it is mainly cleared from the
circulation within 10 to 15 minutes. Except for that portion of the insulin that combines with
receptors in the target cells, the remainder is degraded by the enzyme insulinase mainly in the
liver, to a lesser extent in the kidneys and muscles, and slightly in most other tissues.
This rapid removal from the plasma is important, because, at times, it is as important to turn off
rapidly as to turn on the control functions of insulin.
ACTIONS OF INSULIN
Insulin is concerned with the metabolism of carbohydrate, proteins and fats.
1. on Carbohydrate Metabolism
Increases transport and uptake of glucose by the cells: This is by increasing the
permeability of cell membrane to glucose, particularly liver, muscle and adipose tissues
,by increases the number of glucose transporters. Insulin is not required for glucose
uptake in some tissues such as brain (except hypothalamus), renal tubules, mucous
membrane of intestine and RBCs
Glucose transporters: Usually, glucose is transported into the cells by sodium‐glucose pump.
Most of the cells have another type of transport proteins called glucose transporters (GLUT). So
far, seven types of GLUT are identified (GLUT 1–7). Among these, GLUT4 is insulin sensitive and
it is located in cytoplasmic vesicles. It is present in large numbers in muscle fibers and adipose
cells.
Figure demonstrating insulin receptor and how it activate GLUT molecule

When insulin‐receptor complex is formed in the membrane of such cells, the vesicles containing
GLUT4 are attracted towards the membrane and GLUT4 is released into the membrane. Now,
GLUT4 starts transporting the glucose molecules from extracellular fluid (ECF) into the cell. The
advantage of GLUT4 is that it transports glucose at a faster rate.
Promotes peripheral utilization of glucose
In presence of insulin, glucose which enters the cell is oxidized immediately.(increase activity of
glucokinase).
Promotes storage of glucose – glycogenesis
Insulin promotes the rapid conversion of glucose into glycogen (glycogenesis), which is stored in
the muscle and liver. Insulin activates the enzymes,glycogen synthase and Inhibits
glycogenolysis by inactivating liver phosphorylase.
Inhibits gluconeogenesis
i.e. the formation of glucose from proteins by inhibiting the release of amino acids from muscle
and by inhibiting the activities of enzymes involved in gluconeogenesis
2. on Protein Metabolism
Insulin facilitates the synthesis and storage of proteins by
Facilitating the transport of amino acids into the cell from blood, (valine, leucine,
isoleucine, tyrosine, and phenylalanine.)
Accelerating protein synthesis by influencing the transcription of DNA and by increasing
the translation of mRNA.
Preventing protein catabolism by decreasing the activity of cellular enzymes which act
on proteins.
Preventing gluconeogenesis.
In case of Insulin deficiency
The catabolism of proteins increases.
Increase gluconeogenesis.
Enhanced urea excretion in the urine.
Weakness as well as deranged functions of the organs because of protein wasting.
3. on Fat Metabolism
Actions of insulin on fat metabolism are:

Synthesis of fatty acids and triglycerides: When the quantity of glucose entering the liver
cells is more than can be stored as glycogen or can be used for local hepatocyte
metabolism, insulin promotes the conversion of all this excess glucose into fatty acids.
These fatty acids are subsequently packaged as triglycerides in very‐low‐density
lipoproteins and transported in this form by way of the blood to the adipose tissue and
deposited as fat. i.e. Storage of fat. This is because Insulin inhibits the action of
hormone‐sensitive lipase.
Activation of lipoprotein lipase in the capillary walls of the adipose tissue, which splits
the triglycerides again into fatty acids, a requirement for them to be absorbed into the
adipose cells, where they are again converted to triglycerides and stored.
Insulin Deficiency Causes
Lipolysis of Storage Fat and Release of Free Fatty Acids. This is because of activation of
the enzyme hormone‐sensitive lipase in the fat cells, this leads to hydrolysis of the
stored triglycerides, releasing large quantities of fatty acids and glycerol into the
circulating blood.
Increases Plasma Cholesterol and Phospholipid Concentrations. The excess of fatty acids
in the plasma associated with insulin deficiency also promotes liver conversion of some
of the fatty acids into phospholipids and cholesterol, two of the major products of fat
metabolism. These two substances, along with excess triglycerides formed at the same
time in the liver, are then discharged into the blood in the lipoproteins.
High lipid concentration—especially the high concentration of cholesterol—promotes
the development of atherosclerosis in people with serious diabetes.
Ketosis and Acidosis. In the absence of insulin but in the presence of excess fatty acids in
the liver cells, the carnitine transport mechanism for transporting fatty acids into the
mitochondria becomes increasingly activated. In the mitochondria, beta oxidation of the
fatty acids then proceeds very rapidly, releasing extreme amounts of acetyl‐CoA. A large
part of this excess acetyl‐CoA is then condensed to form acetoacetic acid. Much of
acetoacetic acid is released from the liver that it cannot all be metabolized by the
tissues causing a state of body fluid acidosis.
One more reason for acidosis is that the
ketoacids are excreted in combination with sodium ions through urine (ketonuria).
Sodium is exchanged for hydrogenions, which diffuse from the renal tubules into ECF
adding to acidosis.
Some of the acetoacetic acid is also converted into b‐hydroxybutyric acid and acetone.
These two substances, along with the acetoacetic acid, are called ketone bodies, and
their presence in large quantities in the body fluids is called ketosis.

4. On Growth
Insulin promotes growth of body by its anabolic action on proteins and acts Synergistically with
growth hormone to Promote Growth.
5. on electrolyte:
Insulin causes K+ to enter cells, with a resultant lowering of the extracellular K+ concentration.
This may be due to increases the activity of Na+–K+ ATPase in cell membranes.
Infusions of insulin and glucose significantly lower the plasma K+ level in normal individuals and
are very effective for the temporary relief of hyperkalemia in patients with renal failure.
6. Effect on skeletal muscles:
During much of the day, muscle tissue depends not on glucose for its energy but on fatty acids.
The principal reason for this is that the normal resting muscle membrane is only slightly
permeable to glucose; under two conditions the muscles do use large amounts of glucose.
One of these is during moderate or heavy exercise, because exercising muscle fibers become
more permeable to glucose even in the absence of insulin because of the contraction process
itself.
The second is during the few hours after a meal. At this time the blood glucose concentration is
high and the pancreas is secreting large quantities of insulin. The extra insulin causes rapid
transport of glucose into the muscle cells.
If the muscles are not exercising after a meal and yet glucose is transported into the muscle
cells in abundance, then most of the glucose is stored in the form of muscle glycogen
Insulin Receptor
Insulin receptor is a glycoprotein with a molecular weight of 340,000. It is present in almost all
the cells of the body. On the target cells, insulin binds with the receptor protein and forms the
insulin‐receptor complex. This complex executes the action by activating the intracellular
enzyme system. (Protein kinase).
REGULATION OF INSULIN SECRETION
1. Role of Blood Glucose Level
When blood glucose level is normal (80 to 100 mg/dL), the rate of insulin secretion is low (up to
10 μU/minute). When blood glucose level increases between 100 and 120 mg/dL, the rate of

insulin secretion rises rapidly to 100 μU/minute. When blood glucose level rises above 200
mg/dL, the rate of insulin secretion also rises very rapidly up to 400 μU/minute.
2. Role of Proteins
Excess amino acids in blood also stimulate insulin secretion. Potent amino acids are arginine
and lysin.
3. Role of Lipid Derivatives
The β‐ketoacids such as acetoacetate also increase insulin secretion.
4. Role of Gastrointestinal Hormones
Insulin secretion is increased by some of the gastrointestinal hormones such as gastrin,
secretin, CCK and GIP.
5. Role of Endocrine Hormones
Diabetogenic hormones like glucagon, growth hormone and cortisol also stimulate insulin
secretion, indirectly. Prolonged hypersecretion of these hormones causes exhaustion of β‐cells,
resulting in diabetes mellitus.
6. Role of Autonomic Nerves
Stimulation of parasympathetic nerve to the pancreas (right vagus) increases insulin secretion.
Chemical neurotransmitter involved is acetylcholine. Stimulation of sympathetic nerves inhibits
the secretion of insulin and the neurotransmitter is noradrenaline. However, the role of these
nerves on the regulation of insulin secretion under physiological conditions is not clear.
EFFECTS OF HYPERGLYCEMIA
Hyperosmolality of the blood.
Excretion of the osmotically active glucose molecules entails the loss of large amounts
of water (poly urea). There is an appreciable urinary loss of Na+ and K+ as well.
The resultant dehydration activates the mechanisms regulating water intake, leading to
polydipsia (increase water intake).
The feeding area of the hypothalamus is not inhibited and thus satiety is not sensed so
food intake is increased. (Polyphagia).
For every gram of glucose excreted, 4.1 kcal is lost from the body. Increasing the oral
caloric intake to cover this loss simply raises the plasma glucose further and increases
the glycosuria, so mobilization of endogenous protein and fat stores and weight loss are
not prevented.
When plasma glucose is episodically elevated over time, small amounts of hemoglobin A
are nonenzymatically glycated to form HbAIc. Careful control of the diabetes with
insulin reduces the amount formed and consequently HbA Ic concentration is measured
clinically as an integrated index of diabetic control for the 4‐ to 6‐wk period before the
measurement. As the average amount of plasma glucose increases, the fraction of
glycated hemoglobin increases in a predictable way. This serves as a marker for average
blood glucose levels over the previous months prior to the measurement. It is about 20–
40 mmol/mol (4–5.9 DCCT %) Monitoring HbA
1c
in type 1 diabetic patients may improve
outcomes.
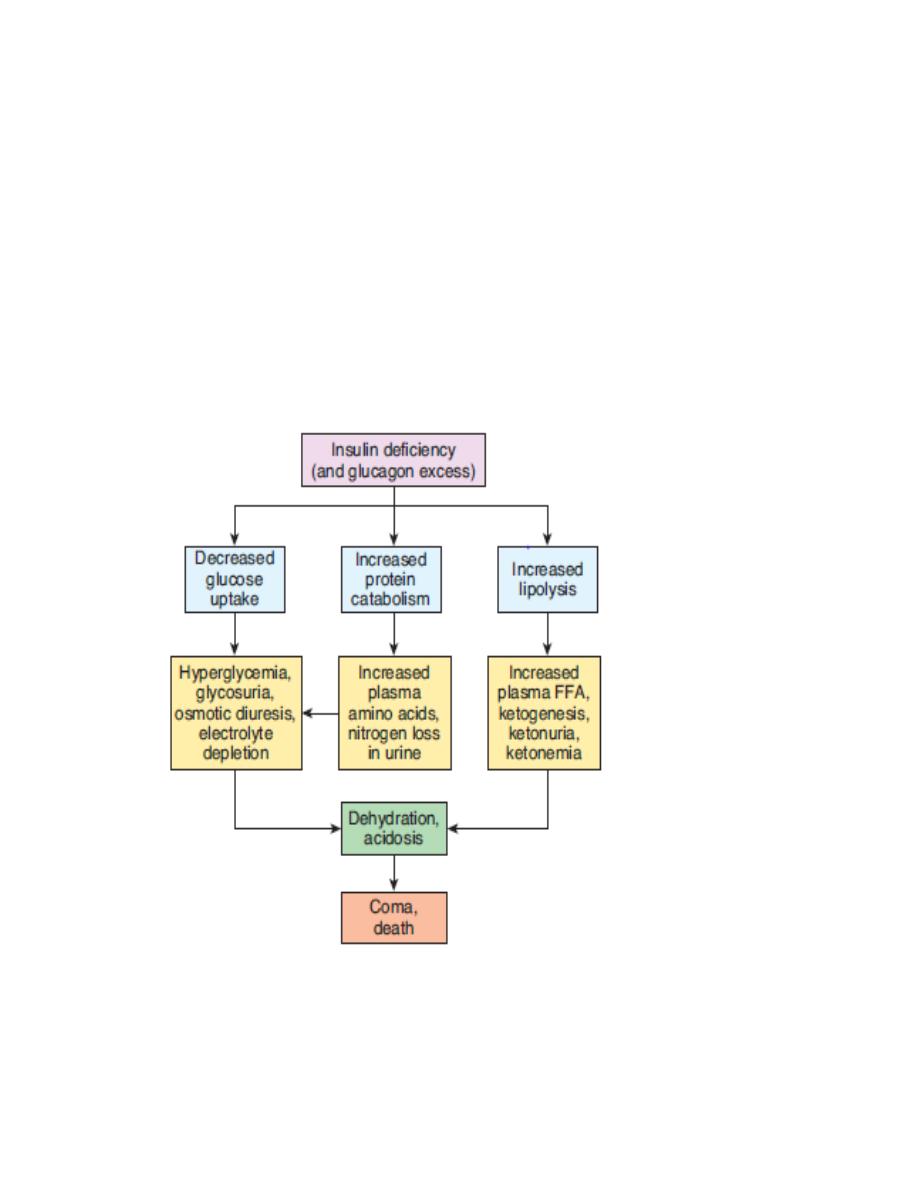
EFFECT OF INSULIN DEFICIANCY(summery):
