Unit 4 - Infectious disease
45
Lecture 4+5+6+7 - Infections caused
by Helminthes
Helminths (from the Greek Helmins, meaning worm) are
large multicellular organisms with complex tissues & organs
They include three groups of parasitic worm, these are:
1- Nematodes or roundworms 2- Trematodes or flukes
3- Cestodes or tapeworms
A) Intestinal human nematodes
Ancylostomiasis (hookworm)
Ancylostomiasis is caused by parasitisation with
Ancylostoma duodenale or Necator americanus.
The adult hookworm is 1 cm long and lives in the
duodenum and upper jejunum attach themselves to the
mucosa of the small intestine by their buccal capsule.
Eggs are passed in the faeces. In warm, moist, shady soil
the larvae develop into rhabditiform and then the infective
filariform stages; they then penetrate human skin and are
carried to the lungs. After entering the alveoli they ascend
the bronchi, are swallowed and mature in the small
intestine, reaching maturity 4–7 weeks after infection. The
worms attach themselves to the mucosa of the small
intestine by their buccal capsule and withdraw blood.
The mean daily loss of blood from one A. duodenale is
0.15 mL and from N. americanus 0.03 mL.
It is one of the main causes of anaemia in the tropics &
subtropics. A. duodenale is endemic in the Far East &
Mediterranean coastal regions & is also present in Africa,
while N. americanus is endemic in West, East & Central
Africa & Central & South America, as well as in the Far East.
Clinical features
1) An allergic dermatitis, usually on the feet (ground itch),
may be experienced at the time of infection.
2) The passage of the larvae through the lungs in a heavy
infection causes a paroxysmal cough with blood-stained
sputum, associated with patchy pulmonary consolidation
and eosinophilia.
3) When the worms have reached the small intestine,
vomiting and epigastric pain resembling peptic ulcer
disease may occur.
4) Sometimes frequent loose stools are passed.
5) The degree of iron and protein deficiency which develops
depends not only on the load of worms but also on the
nutrition of the patient and especially on the iron stores.
Anaemia with high-output cardiac failure may result.
6) The mental and physical development of children may be
retarded in severe infection.
Investigations
1) There is eosinophilia.
2) The characteristic ovum can be recognised in the stool.
3) If hookworms are present in numbers sufficient to cause
anaemia, faecal occult blood testing will be positive and
many ova will be present.
Management
1) A single dose of albendazole (400 mg) is treatment of choice.
2) Alternatively, mebendazole 100 mg 12-hourly for 3 days
may be used. 3) Anaemia and heart failure associated
with hookworm infection respond well to oral iron, even
when severe; blood transfusion is rarely required.
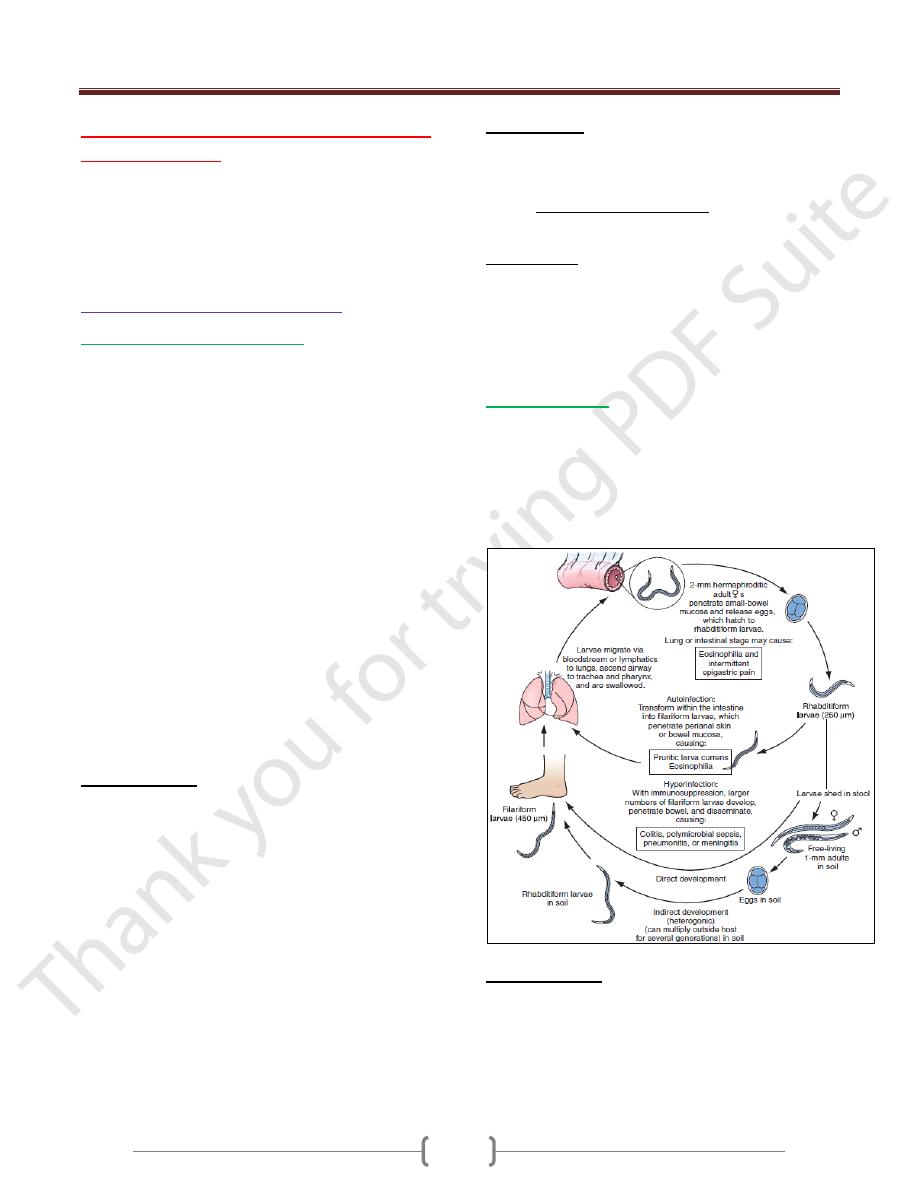
Strongyloidiasis
Strongyloides stercoralis is a very small nematode (2 mm
× 0.4 mm) which parasitises the mucosa of the upper part
of the small intestine, often in large numbers, causing
persistent eosinophilia.
Strongyloidiasis occurs in the tropics and subtropics, and
is especially prevalent in the Far East.
Clinical features
The classic triad of symptoms consists of abdominal pain,
diarrhoea and urticaria.
Cutaneous manifestations, either urticaria or larva currens
(a highly characteristic pruritic, elevated, erythematous
lesion advancing along the course of larval migration), are
characteristic and occur in 66% of patients.

Unit 4 - Infectious disease
46
Systemic strongyloidiasis (the Strongyloides hyper-
infection syndrome), with dissemination of larvae
throughout the body occurs in association with immune
suppression (intercurrent disease, HIV& HTLV-1 infection,
corticosteroid treatment). Patients present with severe,
generalised abdominal pain, abdominal distension &shock.
Massive larval invasion of the lungs causes cough, wheeze
and dyspnoea; cerebral involvement has manifestations
ranging from subtle neurological signs to coma. Gram-
negative sepsis frequently complicates the picture.
Investigations
1) There is eosinophilia.
2) Serology (ELISA) is helpful, but definitive diagnosis
depends upon finding the larvae.
3) The faeces should be examined microscopically for motile
larvae; excretion is intermittent so repeated examinations
may be necessary.
4) Larvae can also be found in jejunal aspirate or detected
using the string test.
5) Larvae may also be cultured from faeces.
Management
1) Ivermectin 200 µg/kg as a single dose, or two doses of
200 µg/kg on successive days, is effective.
2) Alternatively, albendazole is given orally in a dose of 15
mg/kg body weight 12-hourly for 3 days. A second course
may be required.
3) For the Strongyloides hyperinfection syndrome,
ivermectin is given at 200 µg/kg on days 1, 2, 15 and 16.
Ascaris lumbricoides (roundworm)
This pale yellow nematode is 20–35 cm long.
Humans are infected by eating food contaminated with
mature ova.
Ascaris larvae hatch in the duodenum, migrate through
the lungs, ascend the bronchial tree, are swallowed and
mature in the small intestine. This tissue migration can
provoke both local and general hypersensitivity reactions,
with pneumonitis, eosinophilic granulomas, bronchial
asthma and urticaria.
Clinical features
1) Intestinal ascariasis causes symptoms ranging from
occasional vague abdominal pain through to malnutrition.
2) The large size of the adult worm & its tendency to
aggregate & migrate can result in obstructive complications
3) Tropical and subtropical areas are endemic for ascariasis,
and in these areas it causes up to 35% of all intestinal
obstructions, most commonly in the terminal ileum.
4) Obstruction can be complicated further by
intussusceptions, volvulus, haemorrhagic infarction and
perforation.
5) Other complications include blockage of the bile or
pancreatic duct and obstruction of the appendix by adult
worms.
Investigations
1) The diagnosis is made microscopically by finding ova in
the faeces.
2) Adult worms are frequently expelled rectally or orally.
3) Occasionally, the worms are demonstrated
radiographically by a barium examination.
4) There is eosinophilia.
Management
A single dose of albendazole (400 mg), pyrantel pamoate
(11 mg/kg; maximum 1 g), piperazine (4 g) or
mebendazole (100 mg 12-hourly for 3 days) is effective
for intestinal ascariasis.
Patients should be warned that they might expel numerous
whole, large worms.
Obstruction due to ascariasis should be treated with
nasogastric suction, piperazine and intravenous fluids.
Prevention
Community chemotherapy programmes have been used to
reduce Ascaris infection.
The whole community can be treated every 3 months for
several years.
Schoolchildren can be targeted; treating them lowers the
prevalence of ascariasis in the community.
Enterobius vermicularis (threadworm)
This helminth is common throughout the world. It affects
mainly children. After the ova are swallowed,
development takes place in the small intestine, but the
adult worms are found chiefly in the colon.
Clinical features
The gravid female worm lays ova around the anus,
causing intense itching, especially at night. The ova are
often carried to the mouth on the fingers and so
reinfection or human-to-human infection takes place
In females the genitalia may be involved. The adult
worms may be seen moving on the buttocks or in the stool
Investigations
Ova are detected by applying the adhesive surface of
cellophane tape to the perianal skin in the morning. This
is then examined on a glass slide under the microscope.

Unit 4 - Infectious disease
47
Management
A single dose of mebendazole 100 mg, albendazole 400 mg
,pyrantel pamoate (11 mg/kg) or piperazine (4 g) is given &
may be repeated after 2 weeks to control auto-reinfection.
If infection recurs in a family, each member should be
treated as above. During this period all nightclothes and
bed linen are laundered. Fingernails must be kept short
and hands washed carefully before meals. Subsequent
therapy is reserved for those family members who
develop recurrent infection.
Trichuris trichiura (whipworm)
Infections with whipworm are common all over the world
under unhygienic conditions.
Infection is contracted by the ingestion of earth or food
contaminated with ova which have become infective after
lying for 3 weeks or more in moist soil.
The adult worm is 3–5 cm long and has a coiled anterior
end resembling a whip.
Whipworms inhabit the caecum, lower ileum, appendix,
colon and anal canal.
There are usually no symptoms, but intense infections in
children may cause persistent diarrhoea or rectal prolapse,
and growth retardation.
Diagnosis is readily made by identifying ova in faeces.
Treatment mebendazole in doses of 100 mg 12-hourly
for 3–5 days or a single dose of albendazole 400 mg.
Tissue-dwelling human nematodes
Filarial worms are tissue-dwelling nematodes.
Disease is due to the host’s immune response to the
worms (both adult and microfilariae (larva)), particularly
dying worms.
The worms are long-lived; microfilariae survive 2–3 years
and adult worms 10–15 years. The infections are chronic
and worst in individuals constantly exposed to reinfection.
Lymphatic filariasis
Infection with the filarial worms Wuchereria bancrofti
and Brugia malayi is associated with clinical outcomes
ranging from subclinical infection to hydrocele and
elephantiasis.
The infection is widespread in tropical Africa, the North
African coast, coastal areas of Asia, Indonesia and
northern Australia, the South Pacific islands, the West
Indies and also in North and South America.
Pathology
Several factors contribute to the pathogenesis of the disease.
1) Toxins released by the adult worm cause
lymphangiectasia; this dilatation of the lymphatic vessels
leads to lymphatic dysfunction and the chronic clinical
manifestations of lymphatic filariasis, lymphoedema and
hydrocele.
2) Death of the adult worm results in acute filarial
lymphangitis.Lymphatic obstruction persists after death of
the adult worm.
3) Secondary bacterial infections cause tissue destruction.
4) The host response to microfilariae is central to the
pathogenesis of tropical pulmonary eosinophilia.
Clinical features
Acute filarial lymphangitis presents with fever, pain,
tenderness and erythema along the course of inflamed
lymphatic vessels.Inflammation of the spermatic cord,
epididymis and testis is common.
The whole episode lasts a few days but may recur several
times a year. Temporary oedema becomes more persistent
and regional lymph nodes enlarge.
Progressive enlargement, coarsening, corrugation, fissuring
and bacterial infection of the skin and subcutaneous tissue
develop gradually, causing irreversible ‘elephantiasis’.
Tropical pulmonary eosinophilia
It is a complication seen mainly in India and is likely to be
due to microfilariae trapped in the pulmonary capillaries
and destroyed by allergic inflammation.
Patients present with paroxysmal cough, wheeze & fever.
If untreated, this progresses to debilitating chronic
interstitial lung disease.
Investigations of lymphatic filariasis
1) In the earliest stages of lymphangitis the diagnosis is
made on clinical grounds, supported by eosinophilia and
sometimes by positive filarial serology.
2) Microfilariae can be found in the peripheral blood at
night, and either are seen moving in a wet blood film or
are detected by microfiltration of a sample of lysed blood.
By the time elephantiasis develops, microfilariae become
difficult to find.
3) Movement of adult worms can be seen on scrotal ultrasound.
4) PCR-based tests for detection of W. bancrofti DNA from
blood.
Management
1) Treatment of the individual is aimed at reversing and
halting disease progression. Diethylcarbamazine (DEC)
kills microfilariae and adult worms.

Unit 4 - Infectious disease
48
2) A single dose of either ivermectin (200 µg/kg) or
albendazole (400 mg) in combination with DEC (300 mg)
also eliminates microfilariae for 1 year.
Trematodes (flukes)
Schistosomiasis
There are five species of the genus Schistosoma which
commonly cause disease in humans: S. haematobium, S.
mansoni, S. japonicum, S. mekongi and S. intercalatum.
S. haematobium was discovered by Theodor Bilharz in
Cairo in 1861 and the disease is sometimes called
bilharzia or bilharziasis.
Habitat
Adult worms live in the mesenteric veins (S. mansoni, S.
japonicum, S. mekongi, and S. intercalatum) or in the
venous plexus around the lower ends of the ureters & the
urinary bladder (S. haematobium). In these sites, they start
their sexual reproduction by releasing eggs. Once deposited
in the host, eggs may stay in the mesenteric vein, be trapped
in the intestines, escape to the intestinal lumen, and migrate
by portal blood to the liver (S. mansoni, S. japonicum).
Eggs of S. haematobium may be trapped in the intestines &
bladder and may escape to the intestinal or bladder lumen.
Life cycle
After the egg being excreted with feces or urine into fresh
water, the eggs hatch and release ciliated motile miracidia
that penetrates into the snail intermediate host. Following
asexual multiplication in the snail, the development of
cercariae, the infective forms for humans, takes 4 to 7
weeks. After leaving the snails, the cercariae can survive
in fresh water for almost 72 hours. When penetration of
the skin in the human host occurs, the cercariae lose their
tails and change into schistosomula. Schistosomula
migrate to the lungs and, in about 6 weeks, mature to
adult worms and descend to their final habitat.
Pathology
This depends on the species and the stage of infection.
Most disease is due to:
1) The passage of eggs through mucosa .
2) Granulomatous reaction to eggs deposited in tissues.
The eggs of S. haematobium pass mainly through the wall
of the bladder, but may also involve rectum, seminal
vesicles, vagina, cervix and uterine tubes. Eggs of S.
haematobium may leave the vesical plexus and be carried
directly to the lung
S. mansoni and S. japonicum eggs pass mainly through
the wall of the lower bowel or are carried to the liver and
then reach the lungs after the development of portal
hypertension and consequent portasystemic collateral
circulation. In both circumstances egg deposition in the
pulmonary vasculature, and the resultant host response,
can lead to the development of pulmonary hypertension.
Clinical features
1) During the early stages of infection there may be itching
lasting 1–2 days at the site of cercarial penetration
(swimmers itch).
2) Acute schistosomiasis (Katayama syndrome) develops
after a symptom-free period of 3–5 weeks, may present
with allergic manifestations such as urticaria, fever,
muscle aches, abdominal pain, headaches, cough and
sweating.
On examination hepatomegaly, splenomegaly,
lymphadenopathy and pneumonia may be present. These
allergic phenomena may be severe in infections with S.
mansoni and S. japonicum, but are rare with S.
haematobium. The features subside after 1–2 weeks.
Chronic schistosomiasis is due to egg deposition and
occurs months to years after infection. The symptoms and
signs depend upon the intensity of infection and the
species of infecting schistosome.
Schistosoma haematobium
As adult worms can live for 20 years or more. It is highly
endemic in Egypt and East Africa, and occurs throughout
Africa and the Middle East
1) Painless terminal haematuria is usually the first and most
common symptom.
2) Frequency of micturition due to bladder neck obstruction.
3) Later the disease may be complicated by frequent urinary
tract infections, bladder or ureteric stone formation,
hydronephrosis, and ultimately renal failure with a
contracted calcified bladder.
4) Pain is often felt in the iliac fossa or in the loin, and
radiates to the groin.
5) In several endemic areas there is a strong epidemiological
association of S. haematobium infection with squamous
cell carcinoma of the bladder. 6) Intestinal
symptoms may follow involvement of the bowel wall.
Schistosoma mansoni
S. mansoni is endemic throughout Africa, the Middle
East, Venezuela, Brazil and the Caribbean.
Characteristic symptoms begin 2 months or more after
infection.

Unit 4 - Infectious disease
49
They may be slight, no more than malaise, or consist of
abdominal pain and frequent stools which contain blood-
stained mucus.
With severe advanced disease,increased discomfort from
rectal polyps may be experienced.
The early hepatomegaly is reversible, but portal hyper-
tension may cause massive splenomegaly, fatal haema-
temesis from oesophageal varices, or progressive ascites.
Liver function is initially preserved because the pathology
is fibrotic rather than cirrhotic.
Schistosoma japonicum, S. mekongi and S.
intercalatum
The clinical features resemble those of severe infection
with S. mansoni, with added neurological features. The
small and large bowel may be affected, and hepatic
fibrosis with splenic enlargement is usual. Deposition of
eggs or worms in the CNS, especially in the brain or
spinal cord, causes symptoms in about 5% of infections,
notably epilepsy, blindness, hemiplegia or paraplegia.
Investigations
1) There is marked eosinophilia.
2) Serological tests (ELISA) are useful as screening tests but
remain positive after chemotherapeutic cure.
3) In S. haematobium infection, dipstick urine testing shows
blood and albumin.
4) The eggs can be found by microscopic examination of the
centrifuged deposit of terminal stream urine . Ultrasound
is useful for assessing the urinary tract; bladder wall
thickening, hydronephrosis and bladder calcification can
be detected.
5) Cystoscopy reveals ‘sandy’ patches, bleeding mucosa and
later distortion.
6) Sigmoidoscopy may show inflammation or bleeding.
Biopsies should be examined for ova.
Management
1) The object of specific treatment is to kill the adult
schistosomes and so stop egg-laying.
2) Praziquantel is the drug of choice for all forms of
schistosomiasis.
3) Surgery may be required to deal with residual lesions such
as ureteric stricture, small fibrotic urinary bladders, or
granulomatous masses in the brain or spinal cord.
Cestodes (Tapeworms)
Cestodes are ribbon-shaped worms which inhabit the
intestinal tract. They have no alimentary system and
absorb nutrients through the tegumental surface. The
anterior end, or scolex, has suckers for attaching to the
host. From the scolex arises a series of progressively
developing segments, the proglottides, which, when shed,
may continue to show active movements. Cross-
fertilization takes place between segments. Ova, present
in large numbers in mature proglottides, remain viable for
weeks and during this period they may be consumed by
the intermediate host. Larvae liberated from the ingested
ova pass into the tissues, forming larval cysticerci.
Tapeworms cause two distinct patterns of disease either
1-Intestinal infection 2- Systemic cysticercosis.
Taenia saginata (beef tapeworm) and Diphyllobothrium
latum (fish tapeworm) cause only intestinal infection,
following human ingestion of intermediate hosts that
contain cysticerci (the larval stage of the tapeworm).
Taenia solium causes intestinal infection if a cysticerci-
containing intermediate host is ingested, and cysticercosis
(systemic infection from larval migration) if ova are ingested.
Echinococcus granulosus (dog tapeworm) does not cause
human intestinal infection, but causes hydatid disease
(which is analogous to cysticercosis) following ingestion
of ova and subsequent larval migration.
Intestinal tapeworm
Humans acquire tapeworm by eating undercooked beef
infected with the larval stage of T. saginata, undercooked
pork containing the larval stage of T. solium, or
undercooked freshwater fish containing larvae of D.
latum. Usually only one adult tapeworm is present in the
gut but up to ten have been reported.
The ova of T. saginata and T. solium are indistinguishable
microscopically. However, examination of scolex and
proglottides can differentiate between them. T. solium has a
rostellum and two rows of hooklets on the scolex, and
discharges multiple proglottides (3–5) attached together
with lower degrees of uterine branching (approximately
10); T. saginata has only four suckers in its scolex, and
discharges single proglottids with greater uterine branching.
Taenia saginata
Infection with T. saginata occurs in all parts of the world.
The adult worm may be several meters long and produces
little or no intestinal upset in human beings, but
knowledge of its presence, by noting segments in the
faeces or on underclothing, may distress the patient.
Ova may be found in the stool.

Unit 4 - Infectious disease
50
Praziquantel is the drug of choice; niclosamide or
nitazoxanide are alternatives.
Prevention depends on efficient meat inspection and the
thorough cooking of beef.
Taenia solium
T. solium, the pork tapeworm, is common in central
Europe, South Africa, South America and parts of Asia. It
is not as large as T. saginata. The adult worm is found
only in humans following the eating of undercooked pork
containing cysticerci.
Niclosamide, followed by a mild laxative (after 1–2 hours)
to prevent retrograde intestinal autoinfection, is effective
for intestinal infection. Cooking pork well prevents
intestinal infection. Great care must be taken by nurses and
other adults while attending a patient harbouring an adult
worm to avoid ingestion of ova or segments.
Cysticercosis
Human cysticercosis is acquired by ingesting T. solium
tapeworm ova, from either contaminated fingers or food .
The larvae are liberated from eggs in the stomach,
penetrate the intestinal mucosa and are carried to many
parts of the body where they develop and form cysticerci,
0.5–1 cm cysts that contain the head of a young worm.
They do not grow further or migrate.
Common locations are the subcutaneous tissue, skeletal
muscles and brain.
Clinical features
When superficially placed, cysts can be palpated under
the skin or mucosa as pea-like ovoid bodies. Here they
cause few or no symptoms, and will eventually die and
become calcified.
Heavy brain infections, especially in children, may cause
features of encephalitis. More commonly, however,
cerebral signs do not occur until the larvae die, 5–20 years
later. Epilepsy, personality changes, staggering gait or signs
of internal hydrocephalus are the most common features.
Investigations
1) Calcified cysts in muscles can be recognised radiologically.
2) In the brain, however, less calcification takes place and
larvae are only occasionally visible by plain X-ray;
usually CT or MRI will show them.
3) Epileptic fits starting in adult life suggest the possibility
of cysticercosis if the patient has lived in or traveled to an
endemic area.
4) The subcutaneous tissue should be palpated and any
nodule excised for histology.
5) Radiological examination of the skeletal muscles may be
helpful.
6) Antibody detection is available for serodiagnosis.
Management
1) Albendazole, 15 mg/kg daily for a minimum of 8 days,
has now become the drug of choice for parenchymal
neurocysticercosis.
2) Praziquantel is another option, 50 mg/kg in three divided
doses daily for 10 days.
3) Prednisolone, 10 mg 8-hourly, is also given for 14 days,
starting 1 day before the albendazole or praziquantel.
4) In addition, anti-epileptic drugs should be given until the
reaction in the brain has subsided.
5) Operative intervention is indicated for hydrocephalus.
6) Studies from India and Peru suggest that most small
solitary cerebral cysts will resolve without treatment.
Echinococcus granulosus (Taenia echinococcus)
& hydatid disease
Dogs are the definitive hosts of the tiny tapeworm E.
granulosus. The larval stage, a hydatid cyst, normally
occurs in sheep, cattle, camels and other animals that are
infected from contaminated pastures or water. By
handling a dog or drinking contaminated water, humans
may ingest eggs. The embryo is liberated from the ovum
in the small intestine and gains access to the blood stream
and thus to the liver. The resultant cyst grows very slowly,
sometimes intermittently.
Hydatid cyst structure
It is composed of an enveloping fibrous pericyst,
laminated hyaline membrane (ectocyst) and inner
germinal layers (endocyst) which gives rise to daughter
cysts, or germinating cystic brood capsule in which larvae
(protoscolices) develop. Over time some cysts may calcify
and become non-viable.
The disease is common in the Middle East, North and
East Africa, Australia and Argentina.
E. multilocularis, which has a cycle between foxes and
voles, causes a similar but more severe infection, ‘alveolar
hydatid disease’, which invades the liver like cancer.
Clinical features
A hydatid cyst is typically acquired in childhood and may,
after growing for some years, cause pressure symptoms.
These vary, depending on the organ or tissue involved. In
nearly 75% of patients with hydatid disease the right lobe
of the liver is invaded and contains a single cyst. In others a
cyst may be found in lung, bone, brain or elsewhere.

Unit 4 - Infectious disease
51
Investigations
1) The diagnosis depends on the clinical, radiological and
ultrasound findings in a patient who has lived in close
contact with dogs in an endemic area.
2) Complement fixation and ELISA are positive in 70–90%
of patients.
Management
1) Hydatid cysts should be excised wherever possible. Great
care is taken to avoid spillage and cavities are sterilized
with 0.5% silver nitrate or 2.7% sodium chloride.
2) Albendazole (400 mg 12-hourly for 3 months) should also
be used.
3) Albendazole is now often combined with PAIR
(percutaneous puncture, aspiration, injection of scolicidal
agent and re-aspiration) to good effect.
4) Praziquantel 20 mg/kg 12-hourly for 14 days also kills
protoscolices
